Переход - реакция
Cтраница 2
 |
Графическое решение уравнения относительно температуры реагирующей поверхности.| Графическое решение уравнения относительно температуры реагирующей поверхности при условии d ( fcr / drna. [16] |
В положении / появляется возможность перехода реакции в область высоких значений температуры. Дальнейшее увеличение Гоо ( положение 2) соответствует трем возможным температурным уровням и, соответственно, трем скоростям реакции. [17]
Критерии, используемые для предсказания перехода реакций углерода с газами в зону II в случае реакций первого по - рядка, представлены в табл. 4; приведены результаты Тиле [ 100J для плоского и сферического образцов. Переход в зону II осуществляется, когда ф фп, где срц - величина ф для начала зоны II; она составляет 2, 4 или 6 для плоского образца, цилиндра или сферы соответственно. [18]
Коэффициенты диффузии D, соответствующие переходу реакции в диффузионную область, рассчитаны из условия ZJ 2 5 - 10 - 15 ft [ 63, с. [19]
Эти давления и определяют собой пределы перехода реакции во взрывную. Следовательно, условие пределов самовоспламенения эквивалентно условию т со. [20]
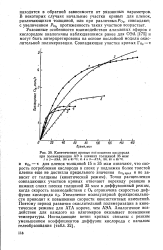 |
Кинетические кривые поглощения кислорода при полимеризации АЭ в пленках толщиной 35 мкм. [21] |
Точки расщепления совпадающих участков кривых отвечают переходу реакции в нижних слоях пленки толщиной 35 мкм в диффузионный режим, когда скорость взаимодействия с О2 ограничена скоростью диффузии кислорода VD. Увеличение молекулярной функциональности приводит к повышению скорости консистентных изменений. [22]
Появление в уравнении третьего члена указывает на переход реакции в диффузионно-кинетическую область вследствие гравитационного перемешивания раствора. На нейтрализацию кислотного раствора до 3 % - ной концентрации при давлении 200 - 300 кгс / см2 и температуре 100 С затрачивается до 30 ч, что в полимиктовых коллекторах также недопустимо. [23]
 |
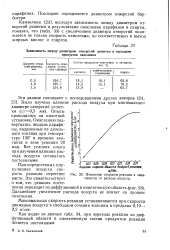
Зависимость константы скорости окисления кокса от температуры. / - кинетическая область. 2 - переходная область - J - внутридиффузионная область. [24] |
Сложная зависимость скорости регенерации от различных факторов и переход реакции из одной области в другую усложняют кинетическое описание процесса в целом. Поэтому рядом авторов разработаны для регенерации уравнения, описывающие скорости окисления кокса в отдельных областях. [25]
Для экспериментального доказательства основного канала рекомбинации носителей при переходе реакции в самоускоряющийся режим проведено исследование влияния предварительной засветки светом 380нм на пороговые характеристики инициирования монокристаллов азида серебра. [26]
 |
Изменение скорости реакции в зависимости от расхода воздуха. [27] |
Как видно из данных табл. 34, при переходе реакции из диффузионной области в кинетическую состав продуктов реакции о стается постоянным. [28]
Условие ф О, таким образом, является условием перехода реакции от медленной к самоускоряющейся. В этом случае реакции разветвления цепи доминируют над реакциями их обрыва. [29]
Совершенно иначе происходит при рассмотрении вариантов, связанных с переходом реакции в диффузионную область по другим компонентам реакции. [30]
Страницы: 1 2 3 4