Переход - фаза
Cтраница 1
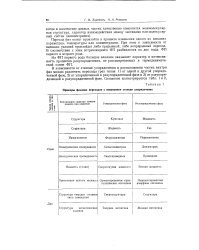 |
Примеры фазовых переходов с изменением степени упорядочения. [1] |
Переход фаз может произойти в процессе изменения одного из внешних параметров, температуры или концентрации. При этом в зависимости от внешних условий произойдет либо прерывный, либо непрерывный переход. В соответствии с этим встречающиеся ФП разбиваются на два вида: ФП первого и второго рода. [2]
Переход фазы через 180 изменяет направление отклонения стрелки прибора. [3]
В установлении точки перехода фазы экспоненциального роста в фазу отрицательного ускорения, безусловно, может существовать субъективизм, связанный с точностью метода определения концентрации - биомассы, а также и с представлениями экспериментатора о степени отклонения экспериментальных данных от расчетного экспоненциального характера роста достаточной, чтобы предположить переход популяции в сферу действия иного закона роста. [4]
 |
Изменение скорости счета при переходе границы ( раздела фаз. а - для неквпящей жидкости. б - для кипящей жидкости. [5] |
При этом в зоне перехода фаз получается максимальный градиент регистрируемой интенсивности излучения. [6]
Условимся начинать отсчет времени в момент перехода фазы 12 через нуль, когда она становится положительной. [7]
В соответствии с реальным механизмом топохимических реакций скорость перехода фаз в катализаторе может определяться как скоростью появления зародышей новой фазы, так и скоростью диффузии атомов в кристаллической решетке и скоростью перестройки последней. [8]
На практике любые течения: газожидкостных смесей сопровождаются переходом фаз. Этот переход наиболее значителен при теплообмене. Компоненты смеси при ее течении термодинамически неравновесны, поэтому такие течения называют неравновесными. Изучение гидродинамики неравновесных течений началось сравнительно недавно. [9]
В соответствии с реальным механизмом топо-химических реакций, скорость перехода фаз в катализаторе может определяться как скоростью появления зародышей новой фазы, так и скоростью диффузии атомов в кристаллической решетке и скоростью перестройки последней. [10]
Любые течения парожидкостных смесей, как правило, сопровождаются переходом фаз. При градиентном адиабатическом течении переход фаз вызывается падением давления и самовскипанием жидкости. Но наиболее значительный переход фаз может возникать при течении с теплообменом между парожидкостной смесью и окружающей средой. Этот процесс сопровождается появлением паровой фазы в недогретой до температуры насыщения жидкости и неравномерным распределением температур и энтальпий в поперечном сечении потока. Причем средние значения температур и энтальпий фаз не равняются их насыщенным значениям. При больших скоростях смеси такое различие увеличивается вследствие отставания времени релаксации от времени протекания процесса. [11]
Большая подвижность ионов в жидкости приводит к резкому ускорению реакций перехода фаз неустойчивых в данных условиях в устойчивые, образованию соединений в твердом виде, по отношению к которым жидкость является уже насыщенной, и их кристаллизации из жидкой фазы. Таким образом, происходит непрерывное растворение тех фаз, по отношению к которым расплав является ненасыщенным, и кристаллизация других устойчивых в данных условиях. Это касается превращений мелких, богатых дефектами строения кристаллов в более крупные, обладающие более правильно построенной кристаллической решеткой. Чем она подвижнее и чем ее строение более благоприятно для перекристаллизации, тем быстрее протекает процесс спекания. Среди последних следует назвать полевой шпат или пегматит, сподумен, магнезиальные соединения и заранее подготовленные плавни. Превышение температуры плотного спекания сопровождается уменьшением уплотнения - вспучиванием. [12]
Если каждый компонент растворим во всех фазах, число реакций перехода ии фазы в фазу равно с - ( Ф - 1) ( см. гл. [13]
Добавление 10 % BaHfO3 и PbHfO3 приводит к понижению температуры перехода низкотемпературной антисегнетоэлектрической фазы в высокотемпературную, что сопровождается аномалией в ходе диэлектрической постоянной и понижением температуры перехода высокотемпературной антисегнетоэлектрической фазы в пара-электрическую. При более высоком содержании BaHfO3 указанных аномалий не наблюдается. Из данных рентгеноструктурных исследований следует, что добавление ВаНЮ3 к РЬШО3 в количестве большем 20 мол. [14]
При дальнейшем нагреве в процессе отпуска закаленной нелегированной стали, как известно, развиваются процессы перехода фаз, полученных при распадении как мартенсита, так и аустенита в нормальный ( кубический) феррит и карбид состава Fe3C с укрупнением последнего ( уменьшением дисперсности) и при непрерывном снижении внутренних напряжений. [15]
Страницы: 1 2 3 4