Таутомерный переход
Cтраница 2
Даны значения t для орто-протонов цикла ХС мета-и пара-протонов менее чувствительных к таутомерному переходу. [16]
В существующих теориях спонтанного, химического и радиационного мутагенеза большое значение придается таутомерным переходам оснований. [18]
В случае некоторых фосфоенолов, например фосфоенолпирува-тов, кроме противоположного резонансного эффекта, существенный вклад в свободную энергию гидролиза вносится таутомерными переходами от енольных форм к более устойчивым кето-формам. В случае таких соединений, как нуклеозид-5 - трифосфаты и в меньшей степени фосфоенолпируваты и нуклеозид-5 - пирофосфаты, определенное значение имеет электростатический эффект, возникающий в результате отталкивания одинаково заряженных групп. Эффекты ионизации и сольватации вызывают ионизацию свободных диссоциирующих групп в продуктах гидролиза. [19]
Оксоанионы более низких ступеней окисления могут отходить от тетраэдри-ческой структуры и переходить в структуры с тремя ковалентными связями только при таутомерном переходе протона от одной из вершин тетраэдра на заряженный отрицательно атом кислорода. [20]
Отсюда ясно, что в дисахаридах первой группы в образовании простой эфирной связи участвуют обе гликозидные гидроксильные группы, вследствие чего их таутомерный переход в карбонильные группы не реализуется. [21]
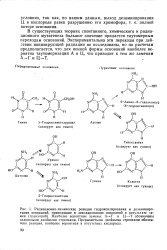
Соединения XXIV интересны тем, что у них нет ни одного атома водорода при азоте, и, следовательно, исключена возможность таутомерных переходов. [22]
Последние два соединения интересны тем, что у них нет ни одного атома водорода при азоте, и следовательно, исключена возможность таутомерных переходов. [23]
Соединения XXIV интересны тем, что у них нет ни одного атома водорода при азоте, и, следовательно, исключена возможность таутомерных переходов. [24]
Соединения ( 37) интересны тем, что у них нет ни одного атома водорода при атоме азота и, следовательно, исключена возможность таутомерных переходов. Поэтому существование двух форм не может иметь другого объяснения, кроме син-анг-изомерии по С1М - связи. [25]
Если один или два атома водорода нетильной группы замещены, значения t оставшегося атома водорода обычно понижены jl ], но изменение t при таутомерном переходе близко к таковому для метальной группы. [26]
Ациклическая форма глюкозы в растворе присутствует в столь незначительных количествах, что не регистрируется физическими методами ( т.е. менее одного процента), но она безусловно есть, ибо не был бы возможен таутомерный переход между а - и ( 3-формами. Указанное выше равновесие устанавливается при растворении чистой a - D-глю-козы в воде через 24 часа. Кроме того, только она - ациклическая форма глюкозы - дает четкие реакции альдегидной группы. В столь же незначительных концентрациях в растворе присутствуют и фуранозные формы глюкозы. [27]
В последующее время нами изучалось взаимодействие неокрашенных ионов многовалентных металлов III, IV, V и VI групп периодической системы с соединениями ди - и полифенольного типа, содержащими одновременно карбонильную группу в орто - или периположении к фенольной, или способными к таутомерному переходу в такие соединения. Применение описанных здесь приемов исследования позволило установить, что содержащие фе-нольный гидроксил органические реактивы могут реагировать с ионами многовалентных элементов по нескольким механизмам. [28]
Мы можем полагать, что изображенные выше формы являются более редкими и в обычных условиях неустойчивыми. Однако таутомерные переходы могут происходить, и притом будут зависеть от рН и температуры. Если они являются причиной ошибок кодирования, то ими могут объясняться некоторые типы мутаций. [29]
При таком строении должно быть возможным получение 4 - и 5-замещен-ных нмидазолов и 3 - и 5-замещенных пиразолов. Однако таких пар изомеров получить не удается вследствие быстрого таутомерного перехода водорода от одного атома азота к другому. В соответствии с этим положения 4 и 5 в имидазоле и положения 3 и 5 в пиразоле должны рассматриваться как практически неразличимые. Эта неоднозначность часто отражается в названиях замещенных гетероциклов такого рода - к цифре, указывающей положение заместителя, добавляется в скобках цифра, указывающая альтернативную возможность отсчета от другого химически неотличимого атома азота, как, например, в 4 ( 5) - метилимидазоле. Только в том случае, когда водород при азоте замещен на менее подвижную группу, например метил, оказывается возможным получить изомерные 4 - и 5-замещен-ные соединения. [30]
Страницы: 1 2 3