Перманга-нат
Cтраница 1
Перманга-нат вводят в виде 15 % - ного водного раствора ( 0 1 - 0 3 % на загрузку) в парафин, нагретый до 120 С. Вода испаряется, а КМп04 диспергируется в парафине. Смесь парафина с катализатором идет в окислительную колонну 3, куда подают очищенный воздух. Температура в окислительной колонне ( 105 - 115 С) поддерживается при помощи нагревающих и охлаждающих змеевиков. Во время индукционного периода ( 2 - 3 ч) в окислительную колонну подводят тепло подачей пара в нижний паровой змеевик. Конденсат в сепараторе 5 отделяется и поступает в сборник 7, а охлажденный воздух направляется в скруббер 6, орошаемый водой, после которого идет в печь для сожжения. [1]
Избыток перманга-ната далее Определяется, во-первых, прибавлением раствора йодистого калия, а за ем титрованием освободившегося иода 1 / 1 Он. [2]
Перренаты, перманга-наты, иодаты, хлооистая ртуть ( I), хлористое олово ( IV) и хлористый цинк также образуют нерастворимые комплексы и будут мешать открытию перхлората. [3]
В процессе ее перманга-нат окисляет ионы. [4]
Иногда применяются также перманга-наты различных металлов или перекись марганца и серная кислота. Наиболее важным практическим способом получения альдегидов является окисление спиртов кислородом воздуха в присутствии металлических катализаторов. Такими катализаторами, действующими уже при обыкновенной температуре, могут служить платина и другие металлы группы платины, а при повышенной температуре - металлическая медь. [5]
 |
Важнейшие характеристики некоторых индикаторов. [6] |
Спектры поглощения растворов перманга-ната и бпхромата значительно отличаются друг от друга ( см. рис. 33, стр. Поэтому можно выделить такой участок спектра, в котором светопоглощение обусловлено только присутствием пер-манганата. По калибровочному графику и оптической плотности исследуемого раствора в этой области спектра находят концентрацию марганца. [7]
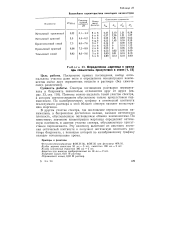 |
Важнейшие характеристики некоторых индикаторов. [8] |
Спектры поглощения растворов перманга-ната и бихромата значительно отличаются друг от друга ( см. рис. 33, стр. Поэтому можно выделить такой участок спектра, в котором светопоглощение обусловлено только присутствием пер-манганата. По калибровочному графику и оптической плотности исследуемого раствора в этой области спектра находят концентрацию, марганца. [9]
Предполагалось, что концентрированные растворы перманга-ната не отличаются с точки зрения удобства обращения с ними и стабильности от более слабых растворов; и полученные данные подтвердили это предположение. [10]
Окисление ненасыщенных углеводородов разбавленным раствором перманга-ната ( нейтральным или щелочным) большей частью заключается в присоединении двух гидроксильных групп по двойной связи с образованием соответствующего гликоля. Дальнейшее окисление перманганатом приводит к разрыву молекулы по месту двойной связи с образованием кислот. Идентификация кислот позволяет определить строение исходного углеводорода. [11]
По окончании окисления восстанавливают избыток перманга-ната этиловым спиртом и кипятят реакционную массу до полного удаления образовавшегося при этом уксусного альдегида. Затем определяют содержание хромата иодометрически: прибавляют кислоту и иодид калия и титруют выделившийся иод раствором тиосульфата. [12]
По количеству затраченного на титрование перманга-ната вычисляют количество закиси меди и затем содержание Сахаров в растворе. [13]
По окончании окисления восстанавливают избыток перманга-ната этиловым спиртом и кипятят реакционную массу до полного удаления образовавшегося при этом уксусного альдегида. Затем определяют содержание хромата иодометрически: прибавляют кислоту и иодид калия и титруют выделившийся иод раствором тиосульфата. [14]
Если при проведении реакции прибавлять избыток перманга-ната, образуется главным образом о-нитробензальдегид. [15]
Страницы: 1 2 3 4