Перхлорат-ион
Cтраница 2
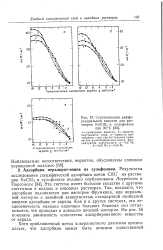 |
Составляющие дифференциальной емкости для растворов NaClO4 в сульфолане при 30 С. [16] |
Адсорбция перхлорат-ионов из сульфолана. Эта система имеет большое сходство с другими системами в водных и неводных растворах. Так, показано, что адсорбция подчиняется или изотерме Фрумкина, или вириаль-ной изотерме с линейной зависимостью стандартной свободной энергии адсорбции от заряда. Как и в других системах, эта неоднозначность вызвана наличием больших боковых сил отталкивания, что приводит к довольно плоской изотерме. На рис. 55 показана зависимость количества адсорбированного вещества от заряда. [17]
Для перхлорат-иона получено значение В - - 0 05 [ 51 а ], и автор объясняет такую малую величину В способностью гидратированного перхлорат-иона разрыхлять или разрушать структуру воды, уменьшая вязкость в окрестности иона. В общем случае такой эффект можно наблюдать только в воде и только для тех ионов, которые в гидратированном состоянии имеют малые эффективные ионные радиусы. [18]
Существенная особенность перхлорат-иона заключается в его очень малой склонности к комплексообразованию с металлами. [19]
Разбавленные растворы перхлорат-иона образуют с метиленовым голубым соединение фиолетового цвета. При концентрации перхлората, превышающей 0 4 %, выделяется хлопьевидный осадок. Реакции мешает также хромат-ион, который, однако, может быть удален ацетатом свинца. [20]
Для определения перхлорат-ионов их восстанавливают до хлорид-ионов и последние обычно определяют методом Фольгарда. [21]
Чувствительность определения перхлорат-иона составляет. [22]
Качественное определение перхлорат-иона в растворе возможно по фиолетово-малиновому осадку перхлората азурина или желтому осадку перхлората сафранина. [23]
Каталитическое влияние перхлорат-иона на алкоголиз является, по Ингольду, значительно более сложным процессом. [24]
В органической фазе перхлорат-ион не взаимодействует с катионами. Перхлораты металлов извлекаются ТОФО [6] плохо, а МДГФО хорошо. [25]
В свободном виде перхлорат-ион, так же как и сульфат-ион, имеет тетраэдрическую конфигурацию, которая несколько искажена в решетке кристалла. Одновременно интенсивность vi становится сопоставимой с интенсивностью разрешенных полос. Эти глубокие изменения в спектре, которые трудно приписать лишь низкой локальной симметрии СЮ - в решетке, авторы объясняют координацией перхлорат-иона. [26]
Другие анионы обнаружению перхлорат-иона не мешают. [27]
Хлорат-ионы в присутствии перхлорат-ионов восстанавливают до хлорид-ионов избытком соли Мора. Избыток соли Мора титруют раствором сульфата церия в присутствии фенилантранило-вой кислоты, затем раствор подщелачивают гидроксидом аммония и выпавший гидроксид железа отфильтровывают. [28]
Броматометрический метод определения перхлорат-ионов основан на осаждении их ацетатом нитрона с последующим определением избытка реагента броматометрическим титрованием. Не мешают определению сульфат -, фосфат, фторид-ионы, а также до 0 1 г-иона хлорида. [29]
Относительная ошибка определения перхлорат-иона в присутствии хлорат - и хлорид-ионов составляет 1 2 - 1 3 % для обоих красителей. [30]
Страницы: 1 2 3 4