Пикрилхлорид
Cтраница 3
Окончательным продуктом нитрования хлорбензола является 2 4 6-тринитрохлорбензол, или пикрилхлорид ( почти бесцветные иглы, темп, плавл. [31]
Окончательным продуктом нитрования хлорбензола является 2 4 6-тринитрохлорбензол, или пикрилхлорид ( почти бесцветные иглы, темп, плавл. [32]
Некоторый интерес может иметь способ получения тринитробензола из тринитрохлорбензола ( пикрилхлорида) по той причине, что исходным сырьем для получения последнего является бензол и, кроме того, нитрование динитрохлорбензола до тринитрохлорбензола осуществляется несколько легче, чем динитробензола до тринитробензола. [33]
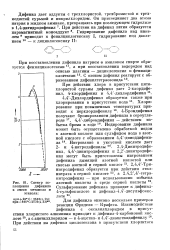 |
Спектр поглощения дифенила в смеси метанола и этанола. [34] |
Дифенил дает аддукты с треххлористой, трехбромистой и трех-иодистой сурьмой и пикрилхлоридом. [35]
Уже давно известно, что некоторые низкомолекулярные вещества, например иод, пикрилхлорид ( 1-хлоро - 2 4 6-тринитробензол) и другие нитросоединения, при парентеральном введении способны вызывать состояние аллергии. Предполагается, что в этом случае аллергия развивается вследствие образования антител не против самих инъицированных веществ, а против их производных. [36]
Полученное соединение идентично с веществом, выделенным по реакции Терпина при обработке щелочью пикрилхлорида и о-аминофенола. [37]
Оказалось, что отношение констант скоростей ацилирования нитрозамещенного и незамещенного амина яара-нитробензоилхло-ридом и пикрилхлоридом ( ПХ) в бензоле в присутствии мостико-вых группировок заметно больше, чем для бифенильной системы. [38]
Наконец, для получения 2 2 4 4 6 6 -гексанитродифенила необходимо вести реакцию конденсации пикрилхлорида только с применением разбавителя, так как при нагревании обоих веществ при 127 и в отсутствии разбавителя они реагируют со взрывом. [39]
На основании результатов анализа ей можно приписать любую из следующих структур: вещества, образованного из пикрилхлорида замещением хлора на метоксигруппу и присоединением молекулы метилата натрия, или же соли, получающейся в результате отрыва протона от первоначально образующегося тринитроанизола и удерживающей при кристаллизации молекулу метанола. При действии этанола он превращается в другую соль, в которой метильная группа заменена на этильную. Возможность отрыва протона из кольца исключается, поскольку Де Бройн [35] показал, что металлический натрий не действует на сылш-тринитробензол в ксилоле даже при температуре кипения растворителя. [40]
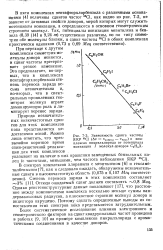 |
Зависимость сдвига частоты Я КР 35С1 ( Av VKOMITJI - чист в комплексах пикрилхлорида от потенциала ионизации I молекул-доноров С6Н5Х. [41] |
Более систематическое исследование влияния электронного и геометрического факторов на сдвиг квадрупольных частот проведено в работах [9, 10] на примере комплексов пикрилхлорида с ароматическими соединениями в качестве доноров. [42]
Поливинилпиридины легко связывают до 90 % пикриновой кислоты; при обработке продуктов реакции РОС13 с 80 % - ным выходом образуется пикрилхлорид. [43]
Исследовано поглощение линейно поляризованного света кристаллами хингидрона [70], комплексом хлоранил - гексаметил-бензол [71], комплексом снлш-тринитробензол - броманил [56] и комплексом пикрилхлорид - гексаметилбензол [72], строение которых установлено методом рентгеноструктурного анализа. При этих исследованиях кристаллы ориентировали так, чтобы наибольшая компонента поляризованного света была направлена сначала перпендикулярно, а затем параллельно плоскостям, в которых расположены кольца компонентов комплекса. Возникающие при возбуждении я-электронов полосы поглощения расположены вблизи ИК-области спектра, причем длина волны больше в том случае, когда вызывающий поглощение свет направлен перпендикулярно плоскостям колец, что совершенно противоположно поглощению света кристаллами чистого бензола. В кристаллах бензола степень я - я-взаймодействия между кольцами очень невелика и п-электронная плотность выше в направлении параллельном, а не перпендикулярном плоскостям колец. [44]
Однако во всех способах очень большой расход серной и азотной кислот, в несколько раз больше теоретически необходимого, что резко повышает себестоимость пикрилхлорида и делает его малодоступным продуктом. В 1946 г. опубликован метод, основанный на взаимодействии пиридинпикрата с фосгеном [24], а позже с хлорокисью фосфора [25], обеспечивающий теоретический выход пикрилхлорида. [45]
Страницы: 1 2 3 4