Пинорезинол
Cтраница 2
Следует отметить, что в исследованных методом озоиолиза образцах ЛМР ( еловом, березовом, эвкалиптовом) не удалось обнаружить структур пинорезинола. Последнее указывает на необходимость дальнейшего исследования природы несопряженных карбонильных групп в лигнине. [16]
Таким путем из кониферилового спирта [ 508; Аг 3 4 - ( МеО) ( НО) СеН3 ] был синтезирован () - пинорезинол [ 509; Аг 3 4 - ( МеО) ( НО) С6Н3 ] 1015 нов, но. Другой путь синтеза состоит в окислении замещенных коричных кислот ( 514), восстановлении образующихся дилактонов ( 511) до тетролов ( 512) и дегидратации последних перегонкой в вакууме или нагреванием с кислыми агентами. [17]
Выделение оптически неактивного пинорезинола как димер-ного промежуточного вещества при энзиматическои дегидрогенизации кониферилового спирта в биосинтезе DHP побудило Фрей-денберга ( 41 ] предположить, что структура пинорезинола содержится в молекуле лигнина. [18]
Наконец, при действии на дихлорироизводное сезамина НС1 Н2О2 был выделен 4 5-дихлор - 1 2-метилендиоксибензол ( 484) Пб2 - пб4) а при взаимодействии пинорезинола с р-нитрофенилдиазонием было получено соединение ( 485) шз. [19]
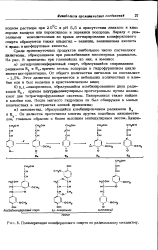 |
Полимеризация кониферилового спирта по радикальному механизму. [20] |
Нь, причем внутримолекулярным прототропным путем возникают две тетрагидрофурановые системы. Пинорезинол также найден в камбии ели. [21]
Представляется сомнительным, чтобы d - пинорезинол был создан растением по схеме, предложенной Фрейденбергом для образования dl - пинорезинола. Если d - пинорезинол образуется из кониферилового спирта, то он должен создаваться особой энзи-матической системой отличной от той, которую предлагает Фрей-денберг. Автору не известно, содержится ли подобное соединение в древесине хвойных пород. Возможно, что оно образуется кратковременно, путем прибавления воды к двойной связи кониферилового спирта. [22]
Аналогичным путем О-диметиловый эфир пинорезинола ( полученный из пинорезинола и щелочного раствора диметилсульфата) и эвдесмин образуют с дымящей азотной кислотой 4 5-динитровератрол ( V), а при окислении перманганатом дают вератровую кислоту. [23]
Попытки выделить дилактон бис ( оксиметил) янтарной кислоты ( получаемый в оптически активной форме из d - пинорезинола при окислении азотной кислотой; XXII) из DHP - dl - P или из лигнина, остались безуспешными. Неудача этих опытов свидетельствует либо о полном отсутствии в молекуле лигнина структуры пинорезинола, либо о незначительном ее количестве, которое с трудом можно обнаружить, либо об изменении этой структуры до такой степени, при которой она не дает более дилактона. Иными словами, эта структура в последнем случае исчезает из молекулы лигнина. [24]
Следует иметь в виду, что в древесине хвойной породы природа создает оптически активный d - пинорезинол. Однако трудно поверить, что растение, создающее оптически активный и неактивный d - пинорезинол, с четырьмя ассимметрическими атомами углерода каждый, использует лишь последнее соединение для образования лигнина. [25]
Для дальнейшего изучения реакционного механизма растворения лигнина с кислым сернистым натрием Энквист и Мойла-нен [34, 36] провели опытные варки с данным реактивом, забу-ференным до рН 7, в течение 72 ч при 100 С. При этом применяли следующие модельные вещества: эвгенол; изоэвгенол; вератрол; ацетованилон; салигенин; салицин ванилин ванилли-ловый спирт; вератровый спирт; 2-окси - 3 5-диметилбензиловый спирт; о-диксиленоловый эфир; пинорезинол; вератровый эфир; метиловый эфир дегидродигидродиизоэвгенола; глицерин - мо-ногваяциловый эфир; ксантон; кониферин и арбутин. [26]
В хлороформенном экстракте были обнаружены пинорезинол и эпинорезинол. [27]
Однако попытки выделить дилактон из DHP - dl - P остались безуспешными. Этим, возможно, объясняется неудача попыток получить дилактон из лигнина хвойных и лиственных пород древесины. По Фрейденбергу [51] же, структура пинорезинола несомненно является составной частью молекулы лигнина в древесине хвойных пород, а сирингорезинола - составной частью молекулы лигнина в древесине твердых пород. [28]
Если бы лигнин образовывался только таким путем, то его состав должен был бы отвечать составу кониферилового спирта без двух или более атомов водорода. Следовательно, образование лигнина частично может происходить и без отщепления водорода. Такое соединение олигоме-ров обеспечивается с помощью промежуточно образующихся хинонметидов, в особенности гипотетического бифункционального хинонметида ( X), представляющего собой промежуточную ступень в образовании пинорезинола. Наряду с этим может также происходить инициированная радикалами полимеризация остатков коричного спирта. Таким образом, принцип полимеризации, приводящей к лигнину, заключается в дегидрировании фенольных групп n - оксикоричных спиртов. Образующиеся радикалы соединяются в промежуточные продукты типа хинонметидов, которые затем стабилизуются с образованием фенольных вторичных структурных элементов ( III) - ( VI) и др. Последние соединяются в высокомолекулярные агрегаты путем дальнейшего дегидрирования с образованием радикалов. На эту реакцию накладывается вторая, заключающаяся в том, что промежуточно возникающие хинонметиды, присоединяясь к уже образовавшимся продуктам, превращаются в устойчивые бензоидные системы. Наряду с этим может происходить дальнейшее увеличение молекулы по типу стирольной полимеризации. [29]
Окислительная деструкция лигнина указывала, что поло-ароматических ядер структурных единиц 5 и 6 должны быть ы С-С - связями с пропановыми цепями другой единицы. Кроме о, оставался открытым вопрос о С-С - связях между боковыми Ьши, а о том, что они возможны, говорила а - у-связь пинорезинола. [30]
Страницы: 1 2 3