Пит-тинг
Cтраница 3
Метод Галлера испытания металлов на кавитационную стойкость, требует небольшого времени для появления кавитационного пит-тинга. [31]
Романов [1] следующим образом характеризует влияние аэрации: В хорошо аэрированных грунтах скорость образования пит-тинга, вначале высокая, быстро замедляется, так как вследствие свободного доступа кислорода окисление железа и осаждение его гидроокиси происходят непосредственно на поверхности металла. Образующаяся при этом защитная пленка способствует понижению скорости питтингоообразования. Кроме того, в плохо аэрированных грунтах наблюдается медленное уменьшение начальной скорости роста питтингов. При этих условиях продукты коррозии, оставаясь в виде соединений двухвалентного железа, либо вообще не защищают, либо обеспечивают весьма незначительную защиту корродирующего металла. Наклон кривой глубина питтин-га - время зависит также от агрессивности данного грунта. [32]
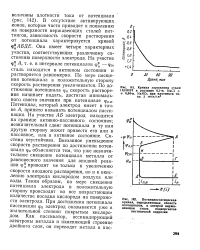
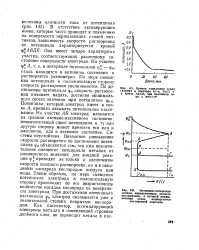
В отсутствие активирующих ионов, которые часто приводят к появлению на поверхности нержавеющих сталей пит-тингов, зависимость скорости растворения от потенциала характеризуется кривой р АБДЕ. Она имеет четыре характерных участка, соответствующих различному состоянию поверхности электрода. По мере смещения потенциала в положительную сторону скорость растворения увеличивается. По достижении потенциала фп скорость растворения начинает падать, достигая минимального своего значения при потенциале фп. Потенциал, который электрод имеет в точке А, принято называть потенциалом пассивации. На участке АБ электрод находится на границе активно-пассивного состояния; незначительный сдвиг потенциала в ту или другую сторону может привести его или в пассивное, или в активное состояние. Внезапное уменьшение скорости растворения по достижении потенциала фп объясняется тем, что уже незначительное смещение потенциала металла от равновесного значения для анодной реакции ф приводит не только к увеличению скорости анодного растворения, но и к окислению электрода кислородом воздуха или воды. Таким образом, по мере смещения потенциала электрода в положительную сторону происходит во все возрастающем количестве посадка кислорода на поверхности электрода. При достижении потенциала пассивации фп электрод оказывается уже в значительной степени покрытым кислородом. [34]
В отсутствие активирующих ионов, которые часто приводят к появлению на поверхности нержавеющих сталей пит-тингов, зависимость скорости растворения от потенциала характеризуется кривой ц АБДЕ. Она имеет четыре характерных участка, соответствующих различному состоянию поверхности электрода. [36]
Введение меди в состав стали не устраняет полностью опасности точечной коррозии, но скорость развития пит-тингов в присутствии меди заметно уменьшается. [37]
Очевидно, что указанные единицы ограничены по своему использованию, если коррозия развивается в виде неравномерно распределенного пит-тинга или ограничена в щелях между опорой и образцом. Это должно быть учтено в дополнителььных записях, описывающих природу и степень локализации коррозии, а также дополнительными данными по действительной глубине питтинга или щелевой коррозии. Отчет должен включать данные по действительным потерям массы и продолжительности испытаний. [38]
 |
Схематическая гальваностатическая анодная кривая. [39] |
Для практики последний пбтенциал даже важнее, так как показывает, что при более отрицательных потенциалах пит-тингов не будет. Для определения фп потенциостатическим методом снимают поляризационную кривую обратного хода. [40]
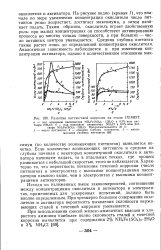 |
Развитие питтинговой коррозии на стали 1Х18Н9Т. [41] |
На рисунке видно ( кривая /), что вначале по мере увеличения концентрации окислителя число пит-тингов резко возрастает, достигает максимума, а затем начинает падать. Таким образом, окислитель играет двойственную роль: при малых концентрациях он способствует активированию процесса во - многих точках поверхности, а при больших - число активных центров уменьшается. Средняя глубина питтинга также растет лишь до определенной концентрации окислителя. [42]
По этой причине можно было полагать, что на образцах с минимальной поверхностью, соизмеримой с размерами характерных реальных пит-тингов, очень быстро будет достигаться полное активирование всей поверхности и, следовательно, сохранение постоянства активной поверхности электрода ( модели питтинга) в течение всего опыта. [43]
Действительно, эксперименты, выполненные на спла-ваз ГРе - Сг [69], показали, что увеличение скорости роста пит-тинга в этой области потенциалов обусловлено деформацией приповерхностных объемов металла и не связано ни с какими поверхностными эффектами или побочными реакциями. [44]
В США широко используется нержавеющая сталь типа 18 / 8, а в Великобритании она всегда разрушается в результате пит-тинга, который проявляется после 7 - 9 месяцев службы и быстро поражает нержавеющую сталь, вероятно, в результате допускаемых условий застоя. [45]
Страницы: 1 2 3 4