Бредиг
Cтраница 1
Метод Бредига из-за высоких температур, создающихся около вольтовой дуги, применим только для получения гидрозолей. [1]
Катализаторы Бредига были, однако, мало применимы к области органических реакций: в присутствии многих органических соединений золи оказывались неустойчивыми. [2]
Появляется работа Бредига и Фаянса [10] об оптически избирательных органических катализаторах. Она содержит первые попытки объяснения стереохимической специфичности ферментов с помощью органических моделей. Так, прежде всего устанавливается, что никотин расщепляет антиподы кам-форкарбоновой кислоты с различной скоростью. [3]
Конденсационный метод Бредига [64], заключающийся в распылении под водой или в органической жидкости таких металлов, как золото, платина, серебро, при помощи вольтовой дуги ( см. стр. Расстояние между электродами обычно регулируется автоматически, и золь перемешивается и охлаждается. [4]
В первоначальном виде метод Бредига применим только к металлам с высокой температурой плавления, не расплавляющимся в условиях опыта. [5]
В монографии Ван Везера37 ошибочно приводится вторая диаграмма Бредига, Франка и Фюльднера как наиболее правильная. [6]
Здесь достаточно напомнить о направлении, начатом работами Бредига [345] по коллоидным растворам металлов как моделям ферментов. [7]
 |
Схема механизма действия катализаторов Си на кварце при асимметрическом разложении рацематов. [8] |
Кун [810; 811], рассматривая механизм стереоспецифического действия катализатора Бредига и Герстнера, подчеркивает, что этот катализатор с большой степенью подобия воспроизводит действие ферментов. На основании имеющейся оптически активной полосы в спектре поглощения группы Hs N сделан вывод о связи этой группы непосредственно с диссимметрическими атомами носителя. Вследствие такой связи группа становится частью диссимметри-ческой молекулы и должна поэтому оказывать асимметризующее воздействие. Следовательно, как полагает Кун, разделить асимметрические и каталитические функции таких образований становится невозможным. Подтверждение того, что сами по себе неактивные молекулы походят на оптически активные, если они диспергированы на оптически активном носителе, Кун находит в примерах ил области неорганической химии. [9]
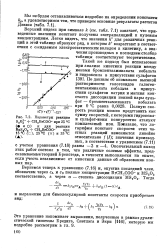 |
Параметры реакции S2 ( 2 - CH2BrCOO - при 25 РС ( и О и для реакции BaSoO, СН. ВгСОО - при. [10] |
Это уравнение напоминает выражения, полученные в рамках дуалистической гипотезы Бредига, Снетлэга и Экри [116], которую мы подробно рассмотрим в гл. [11]
Неоднократно наблюдалось, что устойчивые золи никогда не получаются по методу Бредига, если принять все предосторожности, обеспечивающие высокую степень чистоты металлической проволоки и воды, где образуется дуга, и если сосуд изготовлен из химически устойчивого вещества. Так, например, было замечено, что если получать золь золота в воде, очищенной, как для определений электропроводности, то он оказывается неустойчивым и имеет голубую окраску; прибавление электролита приводит к образованию стабильного красного золя золота. Очевидно, для стабилизации таких золей необходимо некоторое количество примеси электролита. [12]
Дальнейшим, очень важным шагом в области исследования этого вопроса была уже цитированная выше работа Бредига и Зоммера, в которой они показали, что коллоидальные металлы платиновой группы, в частности коллоидальный палладий, так же точно ускоряют реакцию Шардингера, как и свежее молоко. [13]
Кинетика реакции распада90 этилового эфира диазоуксусной кислоты была подвергнута исследованию, причем данные, полученные при адиабатическом нагревании, согласуются с уравнением Бредига и Эпштейна. Куртиус и Мюллер91 нашли, что этил-диметилфумарат можно синтезировать путем нагревания этил-ос-диазопропината. [14]
Страницы: 1 2 3