Сухая пластинка
Cтраница 1
Сухие пластинки опрыскивают раствором нингидрина ( приготовление см. с. На белом фоне пластинки появляются красные или красно-фиолетовые пятна, обусловленные свободными аминогруппами. [1]
Сухие пластинки опрыскивают реактивом Драгендорфа и высушивают при комнатной температуре. Появляются пурпурные или оранжевые пятна холина и холинсодержащих соединений. [2]
Сухие пластинки опрыскивают проявляющим раствором: на бледно-фиолетовом фоне появляются фиолетовые пятна. Проявитель реагирует со всеми фосфолинидами. [3]
Сухую пластинку опрыскивают реактивом и дают снова высохнуть. [4]
Для проявления сухую пластинку опрыскивают 1 А - ным раствороммолибдата аммония в воде, а затем 1 % - ным раствором хлористого олова ( II) в 10 % - ной соляной кислоте. [5]
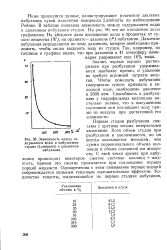 |
Зависимость между содержанием воды в набухаемом студне ( Laminaria и давлением набухания. [6] |
Ниже приводятся данные, иллюстрирующие изменение давления набухания сухой пластинки водоросли Laminaria по наблюдениям Рей Нке. В таблице показана зависимость между содержанием воды и давлением набухания студня. На рис. 96 эти же отношения даны графически. На абсциссе дано поглощение воды в процентах от сухого вещества ( W), на ординате-давление ( Р) набухания. Давление набухания определяется по тому давлению, которое необходимо приложить, чтобы снова выдавить воду из студня. [7]
Для проявления Гх-замещенных производных амино кислот и пептидов 1189 ] сухую пластинку опрыскивали 0 05 % - ным раствором морнпа, нагревали 2 мин. С, и затем пятна обнаруживали в УФ-свете. [8]
Эталонные кривые снимали на тщательно промытых обезжиренных и высушенных в эксикаторе сухих пластинках - В процессе нагружения стопы фиксировали ее суммарную высоту при различных нагрузках. По полученным значениям строили исходную кривую в координатах: деформация в мкм, отнесенная к одной пластине, и напряжение сжатия. Затем стопу разбирали, пластинки повторно промывали, просушивали и для следующего эксперимента смазывали подопытным маслом - свежим или работавшим. [9]
При обнаружении фосфорорганя-ческих пестицидов и других соединений, которые необходимо гидролизовать, опрыскивают сухую пластинку раствором в), покрывают стеклом, нагревают 30 мин при 180 С, опрыскивают раствором а) и снова нагревают 5 мин. Охлаждают, опрыскивают раствором б), помещают в камеру, заполненную парами аммиака, и выдерживают до обесцвечивания фона. Вещества обнаруживаются в виде голубых пятен. [10]
В случае необходимости ( при условии, что анализируемые вещества останутся неизменными) перед тем как охлажденные сухие пластинки помещать в сухую камеру для разделения их следует активировать ( см. также гразд. [11]
Плотности определялись на денситометре конструкция Селаина [2]; они выражены в произвольных единицах ( в см клина прибора) и поэтому их нельзя сравнивать с обычными оптическими плотностями, измеренными на сухих пластинках. [12]
Сухие пластинки опрыскивают аммиачным раствором окиси серебра ( см. работу Гидролиз нуклеопротеидов) и прогревают при 110 С до появления коричневых пятен, обусловленных глицерином и инозитом. [13]
Стеклянные пластинки размером 9X12 см моют хромовой смесью, затем водопроводной и дистиллированной водой и сушат в вертикальном положении. Сухие пластинки перед нанесением сорбционной массы протирают спиртом или эфиром. Для приготовления сорбционной массы берут 35 г силикагеля КСК, просеянного через сито 100 меш, 2 г гипса, 90 мл дистиллированной воды, все переносят в коническую колбу с притертой пробкой и встряхивают в течение 15 мин. Приготовленную массу в количестве 10 г наносят на пластинку и равномерно распределяют по поверхности. [14]
Проявляют, закрепляют и тщательно промывают пластинки. Сухие пластинки устанавливают на столике спектропроектора, проецируют исследуемые спектрограммы на экран спектропроек-тора и приступают к расшифровке. [15]
Страницы: 1 2 3 4