Двухвалентная платина
Cтраница 1
Двухвалентная платина не дает волны восстановления в нейтральных растворах, a Ptlv такие волны дает. Волна Ptlv в 0 3 М растворе нитрата натрия начинается от нулевого напряжения и образует четкое плато около - 0 6 в. Затем, примерно от значения - 0 8 в, кривая начинает резко падать, образуя вторую волну с четким плато при - 1 2 в. Потом ток снова начинает увеличиваться и достигает потенциала разряда катиона электролита. Высота первой волны прямо пропорциональна концентрации Pt в растворе и может поэтому служить для ее количественного определения ( см. пр. [1]
Двухвалентная платина образует нитритные комплексы аналогичных типов. [2]
Двухвалентная платина образует с диэтилдитиофосфатом соединение, точно отвечающее формуле [ ( CzHaO PSSbPt. Растворы диэтилдптиофосфата платины в органических растворителях окрашены в слабый желто-оранжевый цвет и поглощают сильно в ультрафиолетовой и относительно слабо в видимой области спектра. Возможно фотометрическое определение платины, а также весовое ее определение после восстановления до двухвалентного состояния. Платина может вызвать помехи при определении других элементов. [3]
Двухвалентная платина реагирует с тиооксином при комнатной температуре очень медленно. Скорость образования хелата повышается при нагревании раствора до кипения. В области рН 3 5 - 5 0 около 93 % платины ( приблизительно 200 мкг) экстрагируется стехиометрическим количеством реагента. [4]
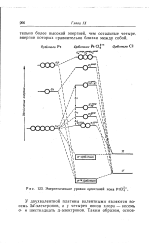 |
Энергетические уровни ороиталей иона PtCl4 -. [5] |
У двухвалентной платины валентными являются восемь Sef-электронов, а у четырех ионов хлора - восемь о - и шестнадцать л-электронов. [6]
Соединения двухвалентной платины иногда содержат во внутренней сфере адденды, которые способны окисляться. В этих случаях процессы, протекающие при взаимодействии с окислителем, существенно осложняются. [7]
Комплексы двухвалентной платины имеют плоскостное строение, а четырехвалентной - октаэдрическое. [8]
Для двухвалентной платины карбонилгалиды гораздо более характерны. С) может быть получен взаимодействием PtC. В бензольном растворе он мономерен и обладает большим дипольным моментом ( и 4 85), что говорит в пользу цис-строения. Водой этот карбонилхлорид быстро разлагается по схеме Pt ( CO) 2Cb Н2О 2НС1 СО2 СО Pt. Известны также аналогичные бромид и иодид. [9]
Для двухвалентной платины карбоннлгалиды гораздо более характерны. С) может быть получен взаимодействием PtCl2 с СО при 150 С. В бензольном растворе он мономерен и обладает большим дипольным моментом ( ц 4 85); что говорит в пользу цис-строения. Водой этот карбонилхлорид быстро разлагается по схеме: Pt ( CO) 2Cb Н2О 2НС1 С02 СО Pt. Известны также аналогичные бромид и иодид. [10]
У двухвалентной платины нельзя ожидать устойчивых комплексов с координационным числом шесть, и она большей частью имеет квадратную конфигурацию. Четырехвалентный ион платины, Pf, имеет только шесть 5 / - электронов и поэтому без особых затруднений образует ковалентные октаэдриче-ские связи с участием двух Sfif-электронов. [11]
Комплексы двухвалентной платины имеют плоскостное строение, а четырехвалентной - октаэдрическое. [12]
Соединения двухвалентных платины и палладия и трехвалентного золота будут подробнее рассмотрены ниже ( стр. [13]
Комплексные соединения двухвалентной платины имеют геометрическую форму плоского квадрата, что определяет их изомерию. [14]
Изомерия соединений двухвалентной платины была известна еще в 40 - х годах прошлого столетня, но только на основе координационной теории она нашла правильное истолкование, причем очень важную роль в этом сыграли соединения дпацидодиампно-вого ряда. [15]
Страницы: 1 2 3 4