Защитная пассивная пленка
Cтраница 1
Защитная пассивная пленка на титане в растворах - H2S04 состоит из сплошного барьерного слоя, прилегающего к металлу, и внешнего менее сплошного слоя. Электрохимическое поведение пассивного титана определяется в основном толщиной и свойствами барьерного слоя. Если барьерный слой формируется пря более положительных потенциалах ( в интервале от 0 14 до 1 4 В) [105], его защитные свойства улучшаются. [1]
При взаимодействии соляной кислоты со сталями не образуется защитной пассивной пленки. Естественная пассивная пленка на кремнистых чугунах, состоящая из Sl02, легко разрушается в соляной кислоте. В растворах кислоты концентрации 2 - 5 % при нормальной температуре иа титаие образуется пассивная пленка, состоящая иэ гидридов титана, но в растворах кислоты ббльшей концентрации она разрушается и титаи переходит в активное состояние. [2]
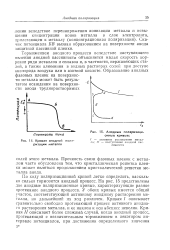 |
Кривая анодной поляризации металла.| Анодные поляризационные кривые. [3] |
Скачок потенциала БВ вызван образованием на поверхности анода защитной пассивной пленки. [4]
Однако стационарный потенциал вследствие большой склонности к образованию защитных пассивных пленок сдвигается в положительную сторону, например в морской воде при 25 С составляет 0 09 в. [5]
Однако стационарный потенциал вследствие большой склонности к образованию защитных пассивных пленок сдвигается в положительную сторону, например в морской воде при 25 С составляет 0 09 В. [6]
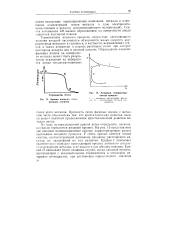 |
Анодные поляризационные кривые. [7] |
Скачок потенциала БВ вызван образованием на поверхности анода защитной пассивной пленки. [8]
При взаимодействии соляной кислоты со сталями не образуется защитной пассивной пленки. [9]
С повышением концентрации окислительных кислот на железоуглеродистых сплавах образуются защитные пассивные пленки. [10]
Высокая коррозионная стойкость хромистых и хромонике-левых сталей обусловлена формированием на их поверхности защитной пассивной пленки. Однако хромоникелевые стали в целом более коррозионно стойки, чем хромистые. [11]
По достижении хорошо известной границы содержания хрома в 12 % на стали образуется защитная пассивная пленка. Характерным для этой пленки является то, что она разрушается в отдельных местах поверхности стали главным образом ионами хлора. [12]
В присутствии этих добавок не только происходит восстановление шестивалентного хрома до трехвалентного, формирующего защитную пассивную пленку, но и одновременно протекает процесс хромирования. [13]
Местом зарождения трещины, как правило, является активный участок поверхности, на котором повреждена защитная пассивная пленка. В результате протекания электохимической коррозии на этом участке образуется повреждение, направленное в глубь металла - питтинг, который, являясь концентратом механических напряжений, дает начало трепщне. [14]
Коррозионная стойкость хромоникелевых сталей ( как и хромистых) обусловлена в основном образованием на поверхности сплава защитной пассивной пленки; однако хромоникелевые стали обладают несколько более высокой. Объясняется это наличием в сплаве никеля, который способствует образованию мелкозернистой однофазной структуры и повышает стойкость стали в разбавленных растворах серной кислоты, а также в ряде водных растворов солей. [15]
Страницы: 1 2 3