Защитная пассивная пленка
Cтраница 3
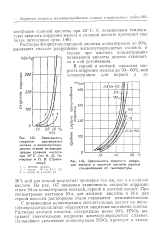
На рис. 147 показана зависимость скорости коррозии стали 20 от концентрации соляной, серной и азотной кислот. При концентрации раствора Юн. С повышением концентрации окислительных кислот на железоуглеродистых сплавах образуются защитные пассивные пленки. Растворы азотной кислоты, содержащие менее 30 % HNO3, вызывают значительную коррозию железоуглеродистых сплавов. [32]
Па рис. 147 показана зависимость скорости коррозии стали 20 от концентрации соляной, серной и азотной кислот. При концентрации раствора Юн. С повышением концентрации окислительных кислот на железоуглеродистых сплавах образуются защитные пассивные пленки. Растворы азотной кислоты, содержащие менее 30 % НМОз, вызывают значительную коррозию железоуглеродистых сплавов. [34]
В связи с тем, что аустенитные стали содержат большое количество никеля и хрома, они обладают повышенным сопротивлением коррозии. Это связано с тем, что при таком легировании и при таком кристаллическом строении аустенит имеет повышенный электрохимический потенциал, что предопределяет повышение его стойкости к электрохимической коррозии. Кроме того, наличие в аустените значительных количеств хрома приводит к образованию на поверхности защитной пассивной пленки. [35]
Из диаграммы Пурбэ следует, что электролитическое окисление металла может иметь также и другие формы. Для этого обычно требуются сильно окислительные условия. Железо, например, сильно разъедается разбавленной азотной кислотой, однако обладает стойкостью в концентрированной азотной кислоте вследствие образования очень тонкой защитной пассивной пленки. В этих условиях железо ведет себя как значительнб более благородный металл, чем является на самом деле, например не вытесняет медь из раствора сульфата меди. [36]
При сопоставлении опытных данных видно, что скорости коррозии с ингибитором и без него практически мало отличаются друг от друга. Из этого следует, что при движении ткани ингибировапле неэффективно ввиду того, что движущаяся ткань уносит адсорбировавшиеся частицы замедлителей коррозии. Еще менее эффективно иигибирование при наложении потенциала анодной защиты, ввиду того, что лри контакте стенки ванны с движущейся тканью защитная пассивная пленка разрушается, и сталь коррозирует с заметной - скоростью - превышающей скорость коррозии в условиях саморастворения. Сварные швы ведут себя аналогично. Для доказательства отсутствия на поверхности стали и сварных швах защитной пассивной пленки при контакте поверхности ванн с движущейся тканью были сняты анодные поляризационные кривые с образцов стали и сварных швов. [38]
Электрохимическое активирование осуществляют на аноде в чистых растворах серной и фосфорной кислот, а также в растворах кислых сернокислых солей при комнатной температуре. Такая обработка особенно рекомендуется перед нанесением относительно толстых ( 50 - 60 мкм и более) слоев никеля. Этот процесс продолжается около 1 мин и заканчивается резким снижением силы тока ( при правильном выполнении условий), что указывает на образование защитной пассивной пленки и повышение анодного потенциала. Перетравливание металла и образование шлама при такой обработке, как правило, не наблюдается. Поверхность стали получается светлой и после тщательного промывания в холодной воде хорошо сцепляется с электролитическим покрытием другими металлами. [39]
При выборе конструкционного материала следует иметь в виду, что некоторые примеси могут интенсифицировать процесс коррозии, и при сопоставимых условиях испытания металлы, устойчивые в чистой кислоте, неприменимы в технической кислоте. Ниже ( табл. 6.3) приводятся экспериментальные данные, показывающие зависимость коррозионной стойкости конструкционных материалов от состава и количества примесей в фосфорной кислоте. Примеси серной и соляной кислот в большей мере интенсифицируют процесс коррозии металлов в фосфорной кислоте, чем добавка азотной кислоты. Это, по-видимому, связано с растворением защитных пассивных пленок на металле, образующихся в чистой фосфорной кислоте. [40]
При сопоставлении опытных данных видно, что скорости коррозии с ингибитором и без него практически мало отличаются друг от друга. Из этого следует, что при движении ткани ингибировапле неэффективно ввиду того, что движущаяся ткань уносит адсорбировавшиеся частицы замедлителей коррозии. Еще менее эффективно иигибирование при наложении потенциала анодной защиты, ввиду того, что лри контакте стенки ванны с движущейся тканью защитная пассивная пленка разрушается, и сталь коррозирует с заметной - скоростью - превышающей скорость коррозии в условиях саморастворения. Сварные швы ведут себя аналогично. Для доказательства отсутствия на поверхности стали и сварных швах защитной пассивной пленки при контакте поверхности ванн с движущейся тканью были сняты анодные поляризационные кривые с образцов стали и сварных швов. [42]
Неравномерность поступления кислорода к отдельным частям металлоконструкций, погруженных в воду, часто служит причиной образования на поверхности металла анодных и катодных участков. Лучше аэрируемый участок становится катодом. Этим объясняется низкая коррозионная устойчивость плохо проваренных, неплотных сварных швов, в которых имеются щели, так как металл в порах и щелях аэрируется хуже, чем другие прилегающие участки поверхности изделия. В этих местах образуются анодные участки, на которых происходит более интенсивное растворение металла. Подобное явление имеет место в металлических конструкциях с закрытыми узкими полостями ( карманами), куда затруднен доступ кислорода и где трудно образоваться защитной пассивной пленке. Влияние различной концентрации кислорода у поверхности металла на распределение анодных и катодных участков в условиях коррозии, идущей с поглощением кислорода, настолько велико, что может действовать намного сильнее, чем структурная неоднородность металла. [43]
Страницы: 1 2 3