Плотность - ток - обмен
Cтраница 2
Плотность тока обмена i0 и коэ4фициент перехода ( 1 - а) являются основными кинетическими характеристиками процесса, ограниченного торможением электрохимической стадии. [16]
Плотности тока обмена в том же электролите были определены, кроме того, Берзинсом и Делахеем 506 ( кривая I) методом гальваностатического замыкания цепи [ по ур. Филыптихом и Делахеем 606 ( кривая 4) из результатов, полученных при потенцио-статическом замыкании цепи [ по ур. Так как теория позволяет пользоваться соответствующими уравнениями только при низких значениях перенапряжения, данные рис. 282 были получены при перенапряжении от 2 до 5 мв. Позднее с помощью метода двойных импульсов Геришер и Краузе496 определили из опытов по гальваностатическому замыканию цепи анодные и катодные кривые плотность тока - напряжение для чистого перенапряжения перехода при больших перенапряжениях. [17]
Плотности токов обмена резко уменьшаются, что приводит к снижению скорости растворения металла. Емкость двойного электрического слоя резко растет, что обусловлено увеличением фарадеевской составляющей. Так как уровень раствора гидроксиламинсульфата в сборниках изменяется, плотность катодного тока может значительно увеличиваться. Кривая заряжения стали 06ХН28МДТ при jK 20 и [ к 10 А / м2 в промышленном растворе гидроксиламинсульфата имеет три пика потенциала, направленные в область положительных значений и свидетельствующие о возможности пассивации стали, однако пассивное состояние быстро нарушается, поэтому значение потенциала электрода колеблется в области активного растворения. [18]
Плотность тока обмена / отвечает скорости прямой и обратной реакции при равновесии. [19]
Плотность тока обмена систем Со ( МН3) б 2, Со ( diam) i ( diam - диамин), Со ( dien) I i 2 увеличивается при возрастании концентрации свободного лиганда по мере образования высших комплексов Co ( NH3) g, Co ( diam) l и Со ( dien) l из соответствующих низших комплексов. [20]
Плотность тока обмена кобальта при возрастании температуры электролита увеличивается и составляет 0 063 А / дм2 при ta 20 С; 0 16 А / дм2 при ta 40 С; 0 35 А / дм2 при ta 60 С и 0 63 А / дм2 при / э 80 С. При возрастании температуры в 4 раза / 0 увеличивается на порядок. [21]
Поэтому плотность тока обмена системы Fe ( CN) - 4 - на золоте, как и на платине, определяется при потенциалах, расположенных положительнее точки нулевого заряда. Поскольку адсорбция кислорода на золоте происходит при более положительных потенциалах, чем на платине [71 ], то в системе Аи j Fe ( CN) i - 4 - вблизи равновесного потенциала на поверхности Au-электрода должны преобладать адсорбированные анионы фонового электролита и молекулы воды. Соответственно, катионы щелочных металлов в этих условиях могут образовывать ассоциаты с адсорбированными анионами. [22]
Сравнение плотностей тока обмена, полученных на тверды. [23]
Значение плотности тока обмена на амальгаме индия невелико, поэтому диффузионные стадии не дают сколько-нибудь заметного вклада в измеряемое перенапряжение. В кислых перхлорат-ных растворах ( до КН кмоль / м3 НС1О4) ионы индия не образуют в заметных количествах комплексов и потенциал амальгамы индия является равновесным. [24]
Величина плотности тока обмена при перезарядке комплексов PtXe -, PtX4 - ( X-Cl, Br, J) на платшювом электроде возрастает при переходе. [25]
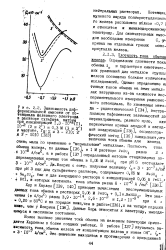 |
Зависимость дифференциальной емкости от потенциала железного электрода в растворе сульфата натрия при концентрации 1 3 10 3 ( 1. [26] |
Определению плотности тока обмена 1Q и параметров кинетических уравнений для металлов группы железа посвящено большое количестве исследований. Однако определение ис тинных токов обмена на этих металлах затруднено из-за сложности экспериментального измерения равновесного потенциала. [27]
Определение плотности тока обмена было приведено выше. Значение р 2 3 RT / aF, где а - константа, а остальные члены имеют обычное значение. [28]
Логарифм плотностей тока обмена различных электродов в зависимости от обратной абсолютной температуры; Из наклона этих, прямых получаются следующие величины энергии активации: электрод № 537 - 6 6 ккал / моль; № 539 - 5 4; № 560 - - 5 5; № 551 - 5 9; № 548 - 5 5 ккал / моль. [29]
Как зависит плотность тока обмена от концентрации потенциалопределяющего вещества. Прологарифмируйте уравнение ( 503) и возьмите производную по логарифму концентрации, от которой зависит также и равновесный потенциал. [30]
Страницы: 1 2 3 4