Электронная плотность
Cтраница 2
Электронная плотность на платине за счет олова возрастает, что способствует падению активности катализатора. Введение рения оказывает иное действие на алюмоплатиновый контакт: число активных центров снижается, а их активность возрастает. Последнее вызвано уменьшением электронной плотности на платине за счет влияния Re, что способствует увеличению активности катализатора. [16]
Электронная плотность в атоме рассчитывается на основании того или иного приближения квантовой механики, и вычисленная величина орбитального радиуса в определенной степени связана с используемым методом расчета. [17]
 |
Связь между характеристиками дефектов и коэффициентом живучести К для железа.| Связь между. [18] |
Электронная плотность в дефектах, ответственных за разрушение от усталости, меняется таким образом, что при изменении К происходит перераспределение электронной плотности. Меньшему значению К соответствует уменьшение плотности электронной проводимости в дефектах и возрастание плотности электронов в ионных остовах на периферии дефектов. Увеличение остовной электронной плотности может привести к увеличению гт - расстояния от центра остова, на котором перекрытие волновых функций позитрона и электрона максимально. Действительно, при уменьшении величины К возрастает гт. [19]
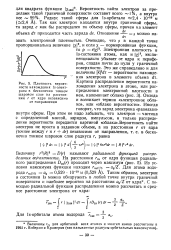 |
Плотность вероятности нахождения ls - элект-рона в бесконечно тонком шаровом слое на расстоянии г от ядра независимо от направления. [20] |
Электронная плотность в ls - состоянии атома, как и xl2, экспоненциально убывает от ядра к периферии, спадая почти до нуля у граничной поверхности. [21]
Электронная плотность на атоме S и энергия напряжения ( 82 81 кдж / молъ, или 19 78 ккал / молъ) тиирано-вого цикла - наименьшие в ряду насыщенных трехчленных гетероциклов. [22]
Электронная плотность в ядре уменьшается, особенно в орта - и пара-положениях. Электрофильный заместитель предпочтительно вступает в мета-поло-жение. Следовательно, заместители второго рода затрудняют по сравнению с бензолом реакции с электрофильными реагентами. [23]
Электронные плотности рассчитаны только на основании коэффициентов при ij3i, tJ32 и ifs, так как эти орбитали заняты в системе с шестью валентными электронами. [24]
Электронная плотность определяется при помощи уравнения, называемого волновым уравнением; оно установлено в 1926 г. Шредингером и описывает волну, присущую электрону. [25]
Электронная плотность р ( г) основного состояния молекулы или твердого тела определяет энергию этого состояния. Однако попытка разбить ее на локализованные капли заряда, центрированные на ядрах или вблизи них, неизбежно приводит к неоднозначности. [26]
Электронная плотность между ядрами теперь значительно меньше, она равна 0 в средней точке, и атомы сильно отталкиваются один от другого. [27]
 |
Схемы пространственного расположения s -, p - и d - атомных. [28] |
Электронная плотность концентрируется на все большем расстоянии по мере того, как значение п растет, и обычно радиальная функция плотности имеет самое большое значение за последней узловой поверхностью. [29]
Электронная плотность, которая рассматривается как вероятность пребывания электрона в данной области молекулы, имеет существенное значение в реакциях, протекающих по ионным механизмам. [30]
Страницы: 1 2 3 4