Автоокисление - углеводород
Cтраница 2
Представления об автоокислении углеводородов, как о цепном процессе, основанные на значительном экспериментальном материале, и факты, показывающие участие в нем свободных радикалов, объясняют кинетическую сторону явления, уточняют вероятные пути активации исходного вещества, предшествующей его химическому взаимодействию с кислородом и разъясняют наблюдаемое при глубоких формах окисления самоускорение процесса, вызываемое автокаталитическим действием промежуточно образующихся перекисей. [16]
Трехокись хрома катализирует автоокисление углеводородов и ненасыщенных алифатических эфиров, восстанавливае т чувствительность фотопластинок, десенсибилизированных метиленовой синью, обладает прижигающим действием, что позволяет использовать ее в медицине. [17]
Но в основном автоокисление углеводородов протекает с образованием гидроперекисей. [18]
Первоначальными промежуточными продуктами автоокисления углеводородов в жидкой фазе при умеренных температурах являются гидроперекиси. [19]
Для механизма дальнейших стадий автоокисления углеводородов важной является установленная на примере трифенилметила легкость присоединения молекулярного кислорода к свободным углеводородным радикалам. И хотя данные о способности других, вчаст-ности высокомолекулярных и низших, алифатических, радикалов реагировать с кислородом пока отсутствуют, можно полагать, что и эти радикалы ведут себя аналогичным образом. [20]
Радикалы RO участвуют в автоокислении углеводородов. [21]
Согласно современным представлениям, процесс автоокисления углеводородов протекает по цепному механизму. Окислительная цепь развивается благодаря накоплению в объеме окисляемых углеводородов свободных радикалов. Первичная активация углеводородов, приводящая к их диссоциации с образованием свободных радикалов, происходит под действием света, температуры, катализатора и других факторов. Образование радикалов дает начало основной цепи окисления. [22]
Современные взгляды на механизм явлений автоокисления углеводородов тесно связаны с представлениями о решающем значении перекисных соединений - свободных перекисных радикалов R - 00 и гидроперекисей R - 00 - Н - в развитии этих процессов. [23]
Большое значение в развитии процесса автоокисления углеводородов несомненно принадлежит образованию свободных радикалов при распаде перекисей. [24]
Современные взгляды на механизм явлений автоокисления углеводородов, обобщенные в i главе, тесно связаны с представлениями о решающей роли перекисей в развитии этих процессов. [25]
Авторы рассматривают действие различных замедлителей автоокисления углеводородов нефтяных масел при добавлении их до начала опыта, а также на различных стадиях развития процесса окисления. [26]
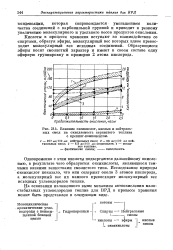 |
Влияние оксикислот, кислых и нейтральных смол на окисляемость сернистого топлива с крекинг-компонентом. [27] |
На основании изложенного выше механизм автоокисления малостабильных углеводородов топлив для ВРД в процессе хранения может быть представлен в следующем виде. [28]
В последнее время изучены реакции автоокисления алкеновых и циклоалкеновых углеводородов, а также насыщенных соединений ( циклоалканов и простых эфиров) в жидкой фазе ( см. гл. Исследование строения образуемых этими соединениями первичных перекисей показало, что они являются результатом присоединения молекулярного кислорода ( по С - Н связи) как к ненасыщенным, так и к насыщенным веществам с сохранением состава и всех деталей структуры исходных молекул ( в том числе двойной связи у алкенов и циклоалкенов) неизменными. [29]
В настоящее время считают, что автоокисление углеводородов атмосферным кислородом является радикально-цепным процессом, в котором в качестве первого стабильного продукта образуется гидропер-оксид. Радикалы в системе, по-видимому, образуются за счет реакции ( 133), а цепной процесс [ реакции ( 134) и ( 135) ] обусловливает превращение углеводорода в его гидропероксид. [30]
Страницы: 1 2 3 4