Трехвалентный плутоний
Cтраница 3
Нерастворимы фторид, оксалат, ферроцианид и гидроокись трехвалентного плутония. Нитрат-ион лишь медленно окисляет трехвалентный плутоний до четырехвалентного и шестивалентного состояния. Окисление до четырехвалентного иона в присутствии нитрит-иона протекает быстро. [31]
С увеличением концентрации азотной кислоты коэффициенты распределения урана и трехвалентного плутония возрастают благодаря высаливающему действию нитрат-иона. Такой же эффект наблюдается для циркония и иттрия. Так как азотная кислота тоже экстрагируется, то с повышением ее концентрации концентрация свободного трибутилфосфата убывает. [32]
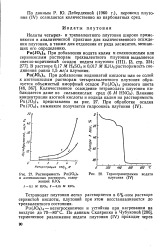 |
Растворимость Ри ( Юз 4 в азотнокислых растворах, содержащих KJO3.| Термогравиграмма иодата плутония ( IV. [33] |
При добавлении иодата калия к солянокислым или сернокислым растворам трехвалентного плутония выделяется светло-коричневый осадок иодата плутония ( III), [ 3, стр. В растворе 0 17 М H2SO4 и 0 017 М KJO3 растворимость соединения равна 1 5 мг / л плутония. [34]
Можно лишь надеяться, что последующие исследования комплексных соединений трехвалентного плутония позволят более подробно охарактеризовать ионРн3 с точки зрения его способности к комплексообразованию. [35]
Восстановление двухвалентным оловом, гидроксиламином, металлическим цинком также приводит к образованию трехвалентного плутония. [36]
Нитрид плутония растворяется на холоду в 3 М H2S04 или НС1 с образованием растворов трехвалентного плутония. Он гидролизуется во влажной атмосфере уже при комнатной температуре, реакция становится быстрой при 100 С. Гидролиз проходит медленно в холодной воде и очень быстро в горячей. [37]
Из окислов плутония в чистом виде получены закись ( моноокись) РиО и двуокись РиО2, наличие окиси трехвалентного плутония РиаО3 доказано лишь косвенными методами, а окись шестивалентного плутония отсутствует даже в виде смешанных окислов. Наиболее устойчива двуокись плутония - коричнево-желтоватый кристаллический порошок, получающийся при прокаливании солей четырехвалентного плутония, а также и солей других валентных состояний. [38]
Оксалат плутония Pu2 ( C2O4) 3 выпадает в виде гидрата Ри2 ( С2О4) з - 9Н2О при действии оксалата натрия на растворы солей трехвалентного плутония. Полное осаждение плутония при концентрации оксалата в маточном растворе 0 2 М достигается через 30 мин. Растворимость оксалата сильно возрастает с увеличением кислотности раствора. [39]
При добавлении кристаллической щавелевой кислоты или ее солей к слабокислым ( 0 3 - 0 8 N) растворам плутония ( III) выпадает малорастворимый оксалат трехвалентного плутония Ри2 ( С2О4) з - 9Н2О [ 3, стр. С повышением кислотности по минеральной кислоте растет растворимость оксалата трехвалентного плутония [ 3, стр. Мешают осаждению сульфаты, фосфаты, фториды, а также трех - и четырехвалентные катионы J9, стр. Осадок оксалата трехвалентного плутония устойчив только в инертной атмосфере. Этот факт в сочетании с малой избирательностью метода не позволяет использовать его в аналитической практике. Методика осаждения Pu2 ( C2O4) з 9Н2О описана на стр. [40]
При рН выше 3 5 этот комплекс термодинамически менее устойчив, чем комплекс с PuIV, так как незакомплексованный Pum окисляется водой до PuIV, который может обмениваться с трехвалентным плутонием. Степень конверсии зависит от скорости реакции обмена всех часгиц, находящихся в растворе, и концентрации свободного плутония. В азотнокислой среде в комплексе происходит частичное окисление Риш до Pulv. В солянокислой среде окисление комплекса идет в меньшей степени. Для стабилизации плутония ( III) используется солянокислый гидроксиламин. [41]
При рН выше 3 5 этот комплекс термодинамически менее устойчив, чем комплекс с Pulv, так как незакомплексованный Риш окисляется водой до PuIV, который может обмениваться с трехвалентным плутонием. Степень конверсии зависит от скорости реакции обмена всех часгиц, находящихся в растворе, и концентрации свободного плутония. В азотнокислой среде в комплексе происходит частичное окисление Риш до Puiv. В солянокислой среде окисление комплекса идет в меньшей степени. Для стабилизации плутония ( III) используется солянокислый гидроксиламин. [42]
Четырехвалентный плутоний из кислых растворов количественно осаждается фениларсоновой кислотой. Трехвалентный плутоний не образует осадка с фениларсоновой кислотой. Оптимальная концентрация азотной и фениларсоновой кислот для избирательного осаждения фениларсоната плутония ( IV) составляет 0 4 - 0 5 и 0 04 - 0 06 М соответственно. Михайлов установил пределы мешающего влияния некоторых элементов при осаждении Pu ( IV) в виде фениларсоната в указанных условиях. [43]
Три-н-октиламин ( ТОА) позволяет эффективно экстрагировать четырехвалентный плутоний из солянокислых [254], азотнокислых [41, 488] и сернокислых [246] растворов. Трехвалентный плутоний не экстрагируется три-н-октиламином. Коэффициент распределения Pu ( IV) зависит от концентрации кислоты и три-н-октиламина. [44]
В ряде химических и физико-химических методов качественного определения плутония используется различие в свойствах валентных форм плутония. Ион трехвалентного плутония в довольно концентрированных водных растворах можно обнаружить по ярко-голубой окраске, резко отличающейся от желто-коричневой окраски водных растворов, содержащих ионы четырехвалентного плутония. [45]
Страницы: 1 2 3 4