Поведение - катализатор
Cтраница 1
Поведение катализаторов, применяемых для переработки угля, должно быть изучено более детально, чтобы установить возможные источники их деградации и разработать меры для их предупреждения. [1]
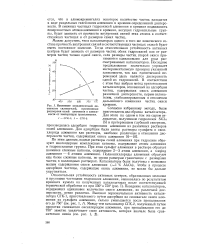 |
Изменение каталитической активности силикагелей, пропитанных растворами солей алюминия в зависимости от температуры прокаливания. [2] |
Поведение катализаторов, содержащих одинаковое количество окиси алюминия, но различной дисперсности, резко различно. [3]
Изучение поведения катализаторов из окислов железа привело В. А. Ройтер а и сотрудников к выводу, что механизм конверсии на них не может быть сведен к последовательному протеканию процессов восстановления окислов железа до металла и окислению последнего парами воды. Измерение скорости каждой из этих реакций порознь показало, что они протекают гораздо медленнее, чем конверсия окиси углерода. Было выяснено, что СО не столько восстанавливает окислы железа, сколько распадается на СО2 и С, в то время как Н2О окисляет в первую очередь уголь, а не металлическое железо. [4]
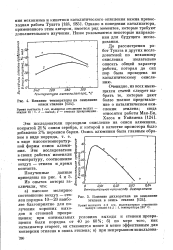 |
Влияние дихлорэтана на окисление этилена в окись этилена. [5] |
Однако в поведении катализатора, примененного этим автором, имеется ряд моментов, которые требуют дополнительного изучения. Ниже указываются некоторые направления для будущего исследования. [6]
Существенные различия между поведением катализаторов при полимеризации в массе и в эмульсии порождаются тем, что при эмульсионной полимеризации каждый растущий полимерный радикал изолирован и концентрацию этих радикалов можно повысить, не опасаясь увеличения скорости обрыва. [7]
Для того чтобы понять поведение катализатора, важно знать его удельную поверхность и распределение пор по размерам. [8]
Таким образом, особенности поведения катализатора йодистый никель - силикагель в реакциях окиси углерода со спиртами, по-видимому, являются весьма общими и совершенно не зависят от природы использованного спирта. Мы полагаем, что активность катализатора йодистый никель - силикагель можно связать с поверхностными комплексами, образование которых требует присутствия следов воды. [9]
Трудно предсказать изменения в поведении катализатора. [10]
На основе данных о поведении перекисных катализаторов следовало ожидать, что скорость автоокисления должна быть пропорциональной концентрации гидроперекиси в степени 0 5 и, следовательно, концентрации абсорбированного кислорода в той же степени. Отсюда следует, что скорость разложения гидроперекиси пропорциональна квадрату концентрации гидроперекиси. Однако при очень низких концентрациях прямая зависимость скорости от количества поглощенного кислорода загибается к началу координат, как следует из рис. 112, так что отрезок, отсекавшийся на рис. 111, не реален. В этой области скорость автоокисления пропорциональна концентрации гидроперекиси в степени 0 5, причем разложение является реакцией первого порядка. Возможно, что это разложение является мономолекулярной реакцией в обоих диапазонах концентраций, за исключением стадии второго порядка, когда активация определяет скорость разложения. [11]
Высказано предположение, что такое поведение катализатора может быть следствием инкорпорирования углеродистых отложений в систему Pt-M и образованием активной субъединицы Pt - M - С. [12]
Высказано предположение, что такое поведение катализатора может быть следствием инкорпорирования углеродистых отложений в систему Pt-M и образованием активной субъединицы Pt - M - С. [13]
В этих таблицах приводятся примеры поведения катализаторов при реакции синтеза, разложения, окисления и гидрогенизации. [14]
Имеется множество противоречивых сведений о поведении катализаторов, полученных на основе экспериментальных данных в ведущих лабораториях мира. [15]
Страницы: 1 2 3 4