Поведение - титан
Cтраница 4
Из данных табл. 14 следует, что в отсутствие окислительных добавок нелегированный титан быстро разрушается, а сплав титана с палладием устойчив в растворах серной и соляной кислот 5 % - ной концентрации. В присутствии кислорода чистый титан устойчив только в растворе, содержащем не более 1 % H2S04, а область устойчивости титана с палладием расширяется до 10 % - ной H2S04 - В растворах, содержащих очень сильный окислитель в виде хлора, а также в горячих растворах фосфорной кислоты, как следует из табл. 13 и 14, не наблюдается большой разницы в поведении титана и сплава титана с палладием. Это определяется коррозионной неустойчивостью самого палладия в этих условиях. [46]
Поэтому титан должен растворяться в кислотах с выделением водорода. Однако на поведение титана в кислотах оказывает сильнейшее влияние состояние его поверхности: окисно-нитридная пленка сдвигает потенциал растворения в положительную сторону. Из-за этого при комнатной температуре титан не растворяется в кислотах азотной и фосфорной любых концентраций и в разбавленных серной и соляной. [47]
Химические свойства элементов подгруппы титана характеризуют преимущественно их металлический характер. В ряду напряжений все три элемента расположены левее водорода. Эта особенность поведения титана и его аналогов обусловлена наличием на их поверхности тонкой пассивирующей пленки оксидов, и в этом отношении они ( особенно титан) напоминают алюминий. [48]
 |
Электрохимические реакции, определяющие основные особенности диаграммы Е - рН для титана. [49] |
Однако общая картина при этом существенно не меняется. В любом случае диаграмма Е - рН дает в общем виде представление о термодинамической устойчивости соединений титана в водных растворах. Но при анализе поведения титана при различных потенциалах или состояниях его поверхности весьма важно помнить, что диаграмма Е - рН указывает только на термодинамическую возможность того или иного процесса. Реальная ситуация будет, естественно, очень сильно определяться кинетическими параметрами рассматриваемых процессов в конкретных условиях. [50]
В качестве основы такого составного электрода помимо титана могут быть использованы тантал, в некоторых случаях цирконий или ниоби-й, а также различные сплавы этих металлов. Однако наибольшее техническое значение по сравнению с другими металлами имеет титан как по электрохимическим и механическим свойствам, так и по доступности. Поэтому настоящая глава посвящена в основном рассмотрению поведения титана, используемого как основа конструкции электрода. Об остальных пленкообразующих металлах ( цирконий, ниобий и тантал) написано менее подробно. [51]
 |
Изменение во времени потенциала титана в 6 н. HoSO4 при 25 С в зависимости от предварительной обработки электрода. л, . [52] |
На образование и свойства оксидной пленки на титане решающее влияние оказывает вода. В работе [78] показано, что титан после выдержки во влажном азоте пассивировался лучше, чем после выдержки в сухом воздухе. Как следует из рис. 2.8, длительность периода активации в серной кислоте также резко возрастает после предварительной выдержки во влажном азоте или воздухе. Особенно большое влияние на поведение титана вода оказывает в органических растворителях. Так, изучение коррозии титана в 2 % - ном растворе брома в метиловом спирте [80] показало, что по мере добавления воды в раствор коррозия из общей становится сначала точечной и при дальнейшем повышении концентрации воды до 30 % совершенно прекращается. [53]
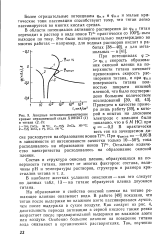 |
Анодные потенциодинамические кривые нержавеющей стали Х18Н10Т ( 1 и титана ( 2, 3. [54] |
На образование и свойства окисной пленки на титане решающее влияние оказывает вода. В работе [49] показано, что титан после выдержки во влажном азоте пассивировался лучше, чем после выдержки в сухом воздухе. Как следует из рис. 4, длительность периода активации в серной кислоте также резко возрастает после предварительной выдержки во влажном азоте или воздухе. Особенно большое влияние на поведение титана вода оказывает в органических растворителях. [55]
В безводных уксуснокислых растворах титан не пассивируется. Анодные поляризационные кривые в широком интервале потенциалов подчиняются уравнению Тафеля с наклоном, близким к 2 3 RTJF. Выход по току при анодном растворении титана близок к 100 % при расчете на Ti ( III) в пределах участка поляризационной кривой ( ( 10 - 3 А / см2) или Ti ( IV) при более высоких потенциалах и плотностях тока. Анодное поведение сплавов на основе титана, но содержащих молибден, существенно отличается от поведения титана. [56]
В безводных уксуснокислых растворах титан не пассивируется. Анодные поляризационные кривые в широком интервале потенциалов подчиняются уравнению Тафеля с наклоном, близким к 2 3 RT / F. Выход по току при анодном растворении титана близок к 100 % при расчете на Ti ( III) в пределах участка поляризационной кривой ( ( 10 - 3 А / см2) или Ti ( IV) при более высоких потенциалах и плотностях тока. Анодное поведение сплавов на основе титана, но содержащих молибден, существенно отличается от поведения титана. [57]
Титан имеет склонность к ползучести уже при комнатной температуре. Заметной становится ползучесть при напряжениях, составляющих 60 % от от. В интервале температур 150 - 350 СС, находясь под нагрузкой, титан перестает ползти. При 350 С ползучесть возникает снова и протекает тем интенсивнее, нем выше температура. Особый характер поведения титана в диапазоне температур 150 - 350 С объясняется старением, происходящим под нагрузкой. [58]
Основное отличие модели растворения титана Капрани от модели Келли заключается, в следующем. Капрани считает, во-первых, в комплексообразовании обязательно принимают участие анионы раствора и, во-вторых, пытается учесть наличие на поверхности активно растворяющегося титана слоя гидрида. Нам представляется, что модель Капрани носит более общий характер и поэтому более справедлива. Важное значение для процессов растворения металлов имеет хемосорбция компонентов раствора на поверхности металла. Ниже при обсуждении особенностей поведения титана в высококонцентрированных растворах хлоридов будут приведены и соответствующие экспериментальные данные о влиянии ас - на активное растворение титана. Естественно, одновременно может происходить параллельное растворение по реакциям (2.1) - (2.5), доля которых в общем балансе должна возрастать в разбавленных растворах. [59]
Совокупность всех трех рассматриваемых критериев поверхностной активности указывает, что титан должен быть поверхностно-активным в железе. Авторы [66] указывают, что введение 2 5 ат. Следовательно, первые порции титана могут действовать как раскислитель, что маскирует истинную природу поведения титана в железе. [60]
Страницы: 1 2 3 4