Поведение - реальный газ
Cтраница 4
Для учета отклонения поведения реальных газов от идеального состояния необходимо ввести корректирующие коэффициенты В m С, причем через В обозначают второй, а через С - третий вириальный коэффициент. [46]
 |
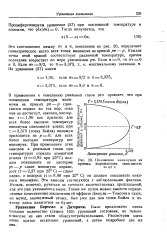
Изотермы углекислого при средних давлениях газа ( pv - p уравнение состояния. [47] |
Для точного описания поведения реальных газов не может быть также использовано уравнение состояния ( 5), предложенное для идеальных газов. [48]
Для математического описания поведения реальных газов предложено много уравнений. [49]
Для учета отклонения поведения реальных газов от идеальных в уравнение состояния вносится поправочный коэффициент, учитывающий объем молекул и силу межмолекулярного взаимодействия. [50]
 |
Положения минимумов на кривых, выражающих зависимость. [51] |
В применении к поведению реальных газов это означает, что при повышении температуры минимумы на кривых pv - р сдвигаются вправо до тех пор, пока они не достигнут, наконец, изотермы т 1 90 как предела; для всех более высоких температур минимумы сдвигаются влево; при т 3 375 ( точка Бойля) минимум э приходится на р 0; для всех й более высоких температур нет минимума. При применении этих выводов к реальным газам при температурах порядка комнатной этилен ( т 0 95 при 25 С) должен показывать на изотерме pv - р сдвиг минимума вправо, азот ( т 2 37 при 25 С) - сдвиг влево, а водород ( т 8 98 при 25 С) не должен показывать никакого минимума. Эти выводы согласуются с наблюдаемыми фактами. Нельзя, конечно, ручаться за точность количественных предсказаний, как это уже указывалось выше. Таким же путем можно вывести определенные качественные заключения об эффекте Джоуля - Томсона в газах, но метод, аналогичный этому, был уже дан для точек Бойля и поэтому здесь излагаться не будет. [52]
Это уравнение удовлетворительно описывает поведение реальных газов при умеренно высоких давлениях, однако не дает точного совпадения с опытными данными. В последнем столбце табл. 13 даны величины pv для ОСЬ при 40 С, вычисленные из уравнения Ван-дер - Ваальса. [53]
Уравнение Вертело неточно описывает поведение реальных газов, но из-за простоты его можно использовать для полуколичественных и качественных оценок. В табл. 6.4 приведены значения у, ДС. RTlny для Н2 и NH3 при различных температурах и давлениях, рассчитанные по уравнению Вертело. [54]
Есть ли доказательства такого поведения реальных газов. [55]
 |
Изображение процесса изотермического сжатия реального газа в координатах.| Изотермы реального газа п координатах V - p. [56] |
Это уравнение качественно отражает поведение реальных газов, включая и область ожижения. [57]
Страницы: 1 2 3 4