Коррозионное поведение - сталь
Cтраница 2
На основании изучения коррозионного поведения стали ЭИ811 в различных кислотных травильных растворах можно заключить, что причиной образования на металле пленки является избирательное растворение б-феррита. Уменьшение скорости коррозии ( катодная поляризация, введение FeSO4 и замедлителей) приводит к уменьшению количества вытравившегося б-феррита, к уменьшению толщины пленки. [16]
Столь небольшие изменения коррозионного поведения стали при погружении в местах, значительно отличающихся по своему географическому положению, могут показаться несколько неожиданными, особенно принимая во внимание существенное различие скоростей атмосферной коррозии. Следует, однако, учитывать, что в тропических водах происходит интенсивное обрастание, способствующее замедлению коррозии. [17]
Влияние малых примесей на коррозионное поведение стали было впервые отмечено примерно 55 лет назад, когда выяснилось, что стали, содержащие медь, обладают повышенной стойкостью в промышленных атмосферах. Позже было установлено, что медьсодержащие стали обладают преимуществами перед нелегированными углеродистыми сталями и в морских атмосферах. [18]
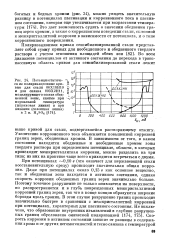
Экспериментальные данные показывают специфические особенности коррозионного поведения стали Х18Н10Т в условиях непрерывного трения ткани по поверхности. При отсутствии контакта с движущейся тканью образцы стали при наложении внешней поляризации пассивируются ( кривые 1 2 3), а при осуществлении контакта с тканью ход поляризационных кривых видоизменяется. Со смещением потенциала к более положительным значениям происходит непрерывное увеличение скорости растворения стали, причем эти значения достигают больших величин. Но это торможение выражено слабо, и область оптимальной запассивированности, характерная для хромоникелевых сталей, отсутствует. На потенциал перепассивации движение ткани существенного влияния не оказывает. [20]
В книге предложены эффективные методы контроля коррозионного поведения сталей, методы исследования структуры и состава коррозионных сред. [21]
Экспериментальные данные по влиянию галоидных ионов на коррозионное поведение стали 1Х18Н9Т при сернокислотном травлении хорошо согласуются с хемосорбционной теорией и, следовательно, подтверждают и дополняют ее. Согласно этой теории [ 3J, [10], галоидные ионы при их добавке в раствор H2SO4, адсорбируясь на поверхности железа, вступают в химическое взаимодействие с поверхностными атомами металла, теряют связь с водной фазой и переходят, таким образом, в состав металлической обкладки двойного электрического слоя. Соединения эти полярны и ориентированы отрицательным полюсом своих диполей в сторону раствора. При достаточных количествах галоидного иона происходит перезарядка поверхности Fe при стационарном потенциале из положительно в отрицательно заряженную, что способствует адсорбции органических катионов и усиливает их замедляющее действие. [22]
 |
Обобщенная зависимость потенциал-коррозия. [23] |
Окислительные свойства азотнокислых растворов в значительной степени определяют коррозионное поведение сталей и прежде всего таких важных конструкционных материалов, как коррозионно-стойкие стали вследствие того, что защитные свойства пассивной пленки, образующейся на них, определяются как раз окислительными способностями раствора. Рост окислительных свойств раствора до определенного значения потенциала ( 1 25 - 1 36 В) приводит к нарушению пассивности и резкому усилению коррозии. Пассивный слой в сильно окислительной среде не нарушается на таких металлах, как титан, цирконий, ниобий, тантал. [24]
Большой цикл испытаний проведен для определения влияния деформаций и напряжений на коррозионное поведение сталей и сплавов в среде N2C4 при высоких температурах и давлениях. [25]
В растворах азотной кислоты более высоких концентраций ( 58 %), коррозионное поведение сталей в отсутствии ионов-активаторов в первую очередь определяется значением потенциалов перехода в состояние перепассивации, так как катодная поляризация осуществляется окислительно-восстановительным процессом при достаточно положительных потенциалах. [26]
Это дает возможность судить о значении обеднения границ зерен хромом, а также о коррозионном поведении стали, склонной к межкристаллитной коррозии в зависимости от потенциала, и о типе коррозионного повреждения. [28]
В результате исследований были выявлены характерные участки анодных поляризационных кривых, дающих необходимую информацию о коррозионном поведении сталей. Сталь 12Х18Н10Т ( Россия) имеет достаточно высокую коррозионную стойкость в области пассивного состояния как в кислых, так и в нейтральных средах. [29]
Азот в виде примесей или дополнительное легирование им в концентрации - 0 15 % оказывает благоприятное влияние на коррозионное поведение хромоникеле-вых сталей, способствуя расширению у-области. Чем выше содержание азота в хромоникелевой стали, тем меньше требуется никеля, чтобы сделать структуру стали полностью аустенитной. Введение - 0 15 % N заменяет от 2 до 4 % Ni и используется в качестве присадки, в основном для сталей типа 18 - 8, что повышает устойчивость аустенита при холодной деформации стали. [30]
Страницы: 1 2 3 4