Химическое поведение - молекула
Cтраница 1
Химическое поведение молекул в возбужденных электронных состояниях - исключительно обширная область для исследования и значительно более трудная для понимания, чем химия основного состояния. Трудность состоит в большем числе реакций, которые становятся возможными, поскольку устраняются термодинамические барьеры, и в переходном характере не только промежуточных продуктов, но и самих реагентов. С этим также связана еще одна проблема: часто мы не знаем, какое возбужденное состояние присутствует в системе и какое состояние является реакционно-способным. [1]
 |
Простейшие изосимметрические изоэлектронные группы а. [2] |
Для понимания химического поведения молекул непременным условием является подсчет числа электронов. Некоторые читатели, возможно, еще не знакомы с этой операцией; поэтому в табл. 1.1 мы приводим подсчет числа электронов для нескольких часто встречающихся фрагментов молекул. [3]
Решающим для химического поведения молекулы углевода является наличие большого числа электроотрицательных групп. Эти группы вызывают соответствующие индукционные эффекты. [4]
Решающим для химического поведения молекулы углевода ( и полиола) является наличие большого числа электроотрицательных групп; эти группы вызывают соответствующие индукционные эффекты. [5]
Исследование факторов, ответственных за химическое поведение молекул, необходимо начинать с изучения фундаментальных законов, которые применимы к таким явлениям. Эти законы могут быть разделены на два типа: 1) термодинамические и статистические законы и 2) квантовомеханические законы. Термодинамические и статистические законы применяются исключительно к группам объектов ( молекул) и поэтому дают количественное описание физических свойств химических веществ. [6]
Функциональные группы обусловливают важнейшие свойства и прежде всего химическое поведение молекул. Изучение спектров молекул показало, что функциональные группы имеют характеристические частоты, мало отличающиеся для отдельных представителей каждого класса органических соединений ( см. гл. [7]
Определенный прогресс имеет место и в прикладных квантовохимических расчетах химического поведения молекул. Проблема реакционной способности является, пожалуй, наиболее трудной в расчетном отношении. Здесь много причин, более подробно об этом будет говориться ниже; собственно, обсуждение этой задачи и составляет содержание данной книги. [8]
Заключительная часть книги посвящена зависимости между пространственными характеристиками и химическим поведением молекул Сахаров и их разнообразных производных типа лактолов, лактонов, циклических ацеталей, ангидросахаров. [9]
Дело в том, что поглощение света может оказать принципиальное влияние на химическое поведение молекулы. После возбуждения знакомые нам атомы могут полностью изменить свое мнение о том, какие валентные углы являются для них наиболее подходящими, функциональные группы могут резко изменить свою реакционную способность, величины констант диссоциации кислот могут измениться на 5 - 10 порядков, степень легкости окисления и восстановления может претерпеть кардинальные изменения, а устойчивые структуры могут стать реакционноспособными. После поглощения энергии молекула переходит в возбужденное высокоэнергетическое состояние, химическое поведение которого описывается гиперповерхностью, совершенно не похожей на поверхность основного состояния, которую химики так хорошо знают. [10]
Расположение и ориентация молекул солюбилизованных веществ весьма важны для понимания природы солюбилизации и физического и химического поведения молекул солюбялизованных веществ. Хотя обычно скорости обмена молекул солюбилизованных веществ между мономер. Таким образом, в зависимости от молекулярной структуры солюбилизата и структуры мицелл следует предположить наличие перераспределения или быстрого взаимного обмена между состояниями с различной ориентацией и энергией. В некоторых случаях требуются определенные локализация и ориентация. Таким образом, можно ожидать различий в локализации чисто гидрофобных растворенных веществ, таких, как гептан, и дифипь - ных растворенных веществ ( полярно-неполярных), таких, как гепта-нол, на структурной основе. Для гептана наиболее вероятно концентрирование в ядре, а гептанол будет располагаться подобно молекулам ПАВ таким образом, что его полярная головка закрепляется на поверхности раздела. [11]
Современное наиболее популярное определение сводится к такой формуле: Под конформационным анализом подразумевается анализ физических свойств и химического поведения молекулы, исходя из геометрии и соотношения 2 различных конформаций, в которых она может существовать [ 50, стр. Очевидно, что изучение как относительной энергетической устойчивости различных конформаций одного и того же соединения, так и свойств последнего как функции его кон-формационного состава и природы отдельных, в первую очередь предпочтительных, конформаций началось раньше, чем Конформационный анализ получил свое наименование и выделился в представляющую самостоятельный интерес область стереохимии. [12]
Реакционная способность реагента, иммобилизованного на электроде, может возрасти или уменьшиться, причем трудно предсказать до какой степени иммобилизация меняет химическое поведение молекул. [13]
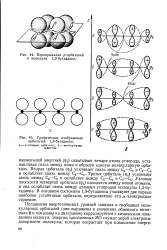 |
Перекрывание р-орбиталей в молекуле 1 3-бутадиена.| Графическое изображение орбиталей 1 3-бутадиена. [14] |
Положения энергетических уровней занятых и свободных молекулярных орбиталей ( они выражены в значениях обменного интеграла Р и показаны на диаграмме) коррелируются с химическим поведением молекул. [15]
Страницы: 1 2 3