Анодное поведение - металл
Cтраница 1
Анодное поведение металлов зависит от многих факторов. К ним прежде всего относится неравномерность структуры массивных отливок, являющаяся следствием ряда условий, в которых протекает процесс огненного рафинирования и затяердевания расплавленного металла. Даже совершенно однородный по составу металлический электрод имеет кристаллы различной величины. [1]
Характер анодного поведения металлов зависит от многих факторов. Металл, растворяющийся под действием анодной поляризации, может при изменении условий потерять эту способность и превратиться в нерастворимый анод. Такое превращение растворимого анода в нерастворимый представляет собой частный случай пассивности металлов. Явление пассивности металлов было открыто М. В. Ломоносовым и описано им в 1738 г. в Диссертации о действии химических растворителей вообще. [2]
Характер анодного поведения металлов зависит от многих факторов. Металл, растворяющийся под действием анодной поляризации, может при изменении условий потерять эту способность и превратиться в нерастворимый анод. Такое превращение растворимого анода в нерастворимый представляет собой частный случай пассивности металлов. Явление пассивности металлов было открыто В. М. Ломоносовым и описано им в 1738 г. в Диссертации о действии химических растворителей вообще. [3]
 |
Анодная кривая для металла. [4] |
Характер анодного поведения металлов зависит от многих факторов. Металл, растворяющийся под действием анодной поляризации, может при изменении условий потерять эту способность и превратиться в нерастворимый анод. Такое превращение растворимого-анода в нерастворимый представляет собой частный случай пассивности металлов. [5]
Характер анодного поведения металлов зависит от многих факторов. Металл, растворяющийся под действием анодной поляризации, может при изменении условий потерять эту способность и превратиться в нерастворимый анод. Такое превращение растворимого анода в нерастворимый представляет собой частный случай пассивности металлов. Явление пассивности металлов было открыто М. В. Ломоносовым и описано им в 1738 г. в Диссертации о действии химических растворителей вообще. [6]
 |
Сравнительная проникающая способность анионов. [7] |
Изучение анодного поведения металлов в присутствии окислителей показывает, что они способствуют сильной анодной поляризации и резко уменьшают критическую плотность тока, при которой металл переходит в пассивное состояние. [8]
Анализ анодного поведения металлов позволяет наметить наиболее рациональные пути уменьшения скорости коррозии или полного подавления коррозионного процесса. [9]
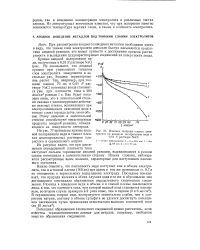 |
Влияние толщины пленки электролита на анодную поляризацию меди в 0 01 N растворе NaCl. [10] |
При рассмотрении анодного поведения металлов необходимо иметь в виду, что тонкие слои электролита довольно быстро насыщаются продуктами анодной реакции; это может привести к достижению предела растворимости и выпадению труднорастворимых соединений на поверхности анода. [11]
В общем случае анодное поведение металлов зависит от их природы, состава электролита, состояния поверхности и величины поляризации. [12]
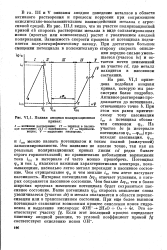 |
Полная анодная поляризационная кривая. [13] |
Ill и V описаны анодное поведение металлов в области активного растворения и процессы коррозии при сопряженном окислительно-восстановительном взаимодействии металла с агрессивной средой. Из рис. 111 1 видно, что на участке поляризационной кривой ab скорость растворения металла в виде сольватированных ионов ( простых или комплексных) растет с увеличением анодной поляризации. Зависимость скорости процесса от потенциала подчиняется полулогарифмическому закону. При достаточно большом смещении потенциала в положительную сторону скорость окисления нередко сильно уменьшается ( участок Ъс) и остается почти неизменной, на участке cd, где металл находится в пассивном состояний. [14]
Влияние механических факторов на анодное поведение металлов исследовалось многими авторами, но только в последнее время опыты начали ставить правильно, так что из них можно делать определенные выводы, имеющие большое значение. [15]
Страницы: 1 2 3