Поверхность - корродирующий металл
Cтраница 3
Необходимым условием электрохимической коррозии является совмещение на поверхности корродирующего металла реакций ионизации и разряда его ионов с какой-либо другой электродной реакцией, протекающей преимущественно в катодном направлении. [31]
 |
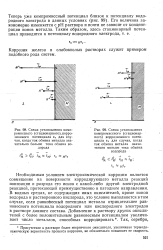
Схема установления компромиссного ( или стационарного коррозионного потенциала 8С, когда ток обмена металла меньше тока обмена водорода. [32] |
Необходимым условием электрохимической коррозии является совмещение на поверхности корродирующего металла реакций ионизации и разряда, его ионов с какой-либо другой электродной реакцией, протекающей преимущественно в катодном направлении. В водных средах, не содержащих иных окислителей, кроме ионов водорода и растворенного кислорода, это условие выполняется в том случае, если равновесный потенциал металла отрицательнее равновесного потенциала водородного или кислородного электродов в растворе данного состава. [33]
Необходимым условием электрохимической коррозии является совмещение на поверхности корродирующего металла реакций ионизации и разряда его ионов с какой-либо другой - электродной реакцией, протекающей преимущественно в катодном направлении. В водных средах, не содержащих иных окислителей, кроме ионов водорода и растворенного кислорода, это условие выполняется в том случае, если равновесный потенциал металла отрицательнее равновесного потенциала водородного или кислородного электродов в растворе данного состава. [35]
Наиболее просто повысить эффективность ингибирования преимущественной блокировкой поверхности корродирующего металла бифункциональными соединениями при их плоскостной ориентационной адсорбции, когда силы отталкивания между заряженными частицами минимальны, а заполнение поверхности значительно. При этом изменение потенциала внутри двойного слоя невелико. [36]
Причины возникновения коррозионных микро - и макропар на поверхности корродирующего металла могут быть самыми различными. [37]
Причины возникновения коррозионных микро - и макро-пар на поверхности корродирующего металла могут быть самыми различными. [38]
Весьма интересна роль сероводорода в изменении молекулярной природы поверхности корродирующего металла. [39]
Важное значение в действии ингибиторов имеет величина заряда поверхности корродирующего металла. Если поверхность металла при коррозии заряжена отрицательно ( например у Fo, AI. Zt), то на ней лучше адсорбируются ингибиторы катионного типа. Если же поверхность металла заряжена положительно, то на яей наиболее вероятна адсорбция ингибиторов анионного типа. [40]
Наблюдается этот вид контроля при легком доступе кислорода к поверхности корродирующего металла, склонности последнего к пассивированию и при большом омическом сопротивлении электролита, например при влажной атмосферной коррозии сталей, которая протекает под очень тонкой пленкой влаги. [41]
Для атмосферной коррозии металлов характерна легкость доступа кислорода к поверхности корродирующего металла, которая обусловлена малой затрудненностью диффузии кислорода тонкими слоями электролита и наличием энергичного самоперемешивания электролита в тонких слоях конвекции. Это приводит к тому, что атмосферная коррозия металлов даже под кислой тонкой пленкой влаги протекает преимущественно с кислородной деполяризацией. Вместе с тем легкость доступа кислорода к поверхности металла облегчает наступление пассивного состояния металла. Таким образом, с уменьшением толщины слоя электролита катодный процесс атмосферной коррозии металла облегчается, а анодный процесс затрудняется. [42]
Важное значение в действии органических ингибиторов имеет величина заряда поверхности корродирующего металла, именуемая ф-по-тенциалом. Максимальная адсорбция органических ингибиторов на поверхности металла наблюдается в области определенных значений р-потенциалов, величина которого близка к потенциалу нулевого заряда металла, так называемой нулевой точке металла. [43]
Важное значение в действии органических ингибиторов имеет величина заряда поверхности корродирующего металла, именуемая р-по-тенциалом. Максимальная адсорбция органических ингибиторов на поверхности металла наблюдается в области определенных значений р-потенциалов, величина которого близка к потенциалу нулевого заряда металла, так называемой нулевой точке металла. [44]
В связи с этим кислород воздуха достаточно легко проникает к поверхности корродирующего металла. Отсюда следует, что с уменьшением толщины слоя электролита катодный процесс атмосферной коррозии металла облегчается, а анодный процесс затрудняется. Таким образом, малая толщина слоя электролита приводит к большому омическому сопротивлению при работе коррозионных микропар. Следовательно, для атмосферной коррозии контролирующим фактором является катодно-анодно-омический контроль. [45]
Страницы: 1 2 3 4