Поверхность - твердый адсорбент
Cтраница 1
Поверхность твердого адсорбента имеет многочисленные ультрамикроскопические выступы и углубления. У атомов, находящихся на выступах, не использованы силы электростатического взаимодействия, вследствие чего они способны к взаимодействию с атомами или молекулами из окружающей среды. Участки поверхности, способные к адсорбции, называются активными центрами. [1]
Адсорбция ионов на поверхности твердых адсорбентов в противоположность молекулярной ( физической) адсорбции в большинстве случаев является необратимой активированной адсорбцией. Иногда она представляет собой обычную химическую реакцию. Поэтому при повышении температуры величина адсорбции ионов в противоположность молекулярной адсорбции нередко увеличивается. [2]
В большинстве случаев поверхность твердого адсорбента энергетически неоднородна ( гл. I) - она представляет собой серию элементарных площадок, обладающих различной теплотой адсорбции. Конечно, площадки с разной величиной q беспорядочно расположены на поверхности адсорбента. Но при выводе уравнения Ленгмюра было предположено, что частицы адсорбата не действуют друг на друга. Поэтому порядок расположения элементарных площадок с различными величинами q не имеет значения. [3]
Процесс адсорбции газа на поверхности твердого адсорбента при постоянной температуре представляет собой процесс изотермического его сжатия. [4]
Поскольку в адсорбции на поверхности твердого адсорбента участвует лишь поверхностный слой атомов адсорбента; Tie. [5]
Явление адсорбции газа на поверхности твердого адсорбента обусловливается силами взаимодействия между молекулами адсорбируемого газа и молекулами адсорбента, следовательно, силами взаимодействия двух сортов молекул. [6]
Явление адсорбции золей на поверхности твердых адсорбентов очень напоминает адсорбцию из настоящих растворов. В то время как гидрофобные золи адсорбируются на поверхности преимущественно благодаря разнице знаков электрических зарядов поверхности и частицы, у гидрофильных золей явление адсорбции на границе твердой фазы происходит благодаря поверхностной активности этих гидрозолей. При малых концентрациях наблюдается нормальная изотерма адсорбции; при больших концентрациях, когда поверхность становится насыщенной, изотерма проходит через максимум. При адсорбции на твердой поверхности также имеют место необратимые процессы и наблюдаются случаи денатурации белков. [7]
Адсорбция из растворов на поверхности твердых адсорбентов отличается от адсорбции индивидуальных веществ ( газов, паров, чистых жидкостей) тем, что в растворе имеется по крайней мере два. Вследствие этого компоненты раствора в этом слое при изменении концентрации вытесняют друг друга, что является характерной особенностью адсорбции из растворов. Таким образом, ни в поверхностном растворе ( в адсорбционном слое), ни в объеме раствора свободных мест нет, происходит лишь вытеснение молекул одного компонента молекулами другого. [8]
Адсорбция из растворов на поверхности твердых адсорбентов отличается от адсорбции индивидуальных веществ ( газов, паров, чистых жидкостей) тем, что в растворе имеется по крайней мере два компонента, образующих на поверхности плотный слой. Вследствие этого компоненты раствора в этом слое при изменении концентрации вытесняют друг друга, что является характерной особенностью адсорбции из растворов. Таким образом, ни в поверхностном растворе ( в адсорбционном слое), ни в объеме рас - твора свободных мест нет, происходит лишь вытеснение молекул одного компонента молекулами другого. [9]
 |
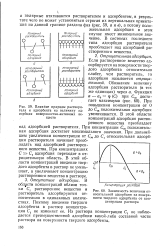
Структурная кривая ( а и кривая распределения объема пор по значениям эффективных радиусов ( б для силикагеля. [10] |
Адсорбция из растворов на поверхности твердых адсорбентов отличается от адсорбции индивидуальных веществ ( газов, паров, чистых жидкостей) тем, что в растворе имеется по крайней мере два компонента, образующих на поверхности плотный слон. Вследствие этого компоненты раствора в этом слое при изменении концентрации вытесняют друг друга, что является характерной особенностью адсорбции из растворов. [11]
Избирательное поглощение молекул вещества поверхностью твердого адсорбента происходит вследствие воздействия на молекулы целевого компонента неуравновешенных поверхностных сил адсорбента. Различают физическую адсорбцию, вызываемую силами молекулярного взаимодействия, и химическую адсорбцию ( хемосорбцию), при которой молекулы поглощаемого вещества вступают в химическую реакцию с молекулами на поверхности адсорбента. В отличие от физической адсорбции лри хемосорбции поглощенные поверхностью молекулы не сохраняют индивидуальность. [12]
Если растворенное вещество адсорбируется на поверхности твердого адсорбента относительно слабее, чем растворитель, то адсорбция называется отрицательной. Обозначим величину адсорбции растворителя ( в тех же единицах) через а. При повышении концентрации от О до Ст положительная адсорбция увеличивается. [14]
Величину адсорбции растворенного вещества на поверхности твердого адсорбента определяют опытным путем введением одинаковых количеств адсорбента в одинаковые объемы растворов разной концентрации или введением разных количеств адсорбента в одинаковые объемы растворов одинаковой концентрации. [15]
Страницы: 1 2 3 4