Внутренняя поверхность - зерно
Cтраница 3
Если процесс тормозится транспортом вещества не к внешней, а к внутренней поверхности контакта, например к внутренней поверхности зерен твердого пористого катализатора, то необходимо учитывать скорость тормозящей стадии - внутреннего транспорта. В этом случае модель усложняется, так как концентрации С / вн и температура Тш изменяются по поверхности контакта в зависимости от радиуса зерна контактного материала R. Скорость внутреннего транспорта можно описать законами Фика и Фурье, применив эффективный коэффициент внутренней диффузии /); эф и эффективный коэффициент теплопроводности лэф. [31]
Метод кип я щ его слоя позволяет прежде всего повысить интенсивность работы катализатора [10, 12, 15-17] за счет полного использования внутренней поверхности зерен и улучшения температурного режима работы. Применение мелких зерен катализатора d C 1 5 мм дает возможность почти полностью снять внутри-диффузионные торможения, характерные для неподвижного слоя. Поскольку энергия активации реакции окисления SO2 на обоих катализаторах была почти одинакова, повышение интенсивности работы катализатора кипящего слоя следует отнести за счет более полного использования внутренней поверхности. [32]
Сте-ень внутреннего диффузионного торможения гетерогенных каталитических процессов зависит от соотношения между скоростью реакции и скоростью транспорта реактантов к внутренней поверхности зерен контакта. Соотношение это определяется не только температурой, давлением реакционной смеси, удельной активностью, макроструктурой и размером зерен катализатора, но и концентрациями веществ, участвующих в реакции. [33]
Сте-ень внутреннего диффузионного торможения гетерогенных каталитических процессов зависит от соотношения между скоростью реакции и скоростьп транспорта реактантов к внутренней поверхности зерен контакта. Соотношение это определяется не только температурой, давлением реакционной смеси, удельной активностью, макроструктурой и размером зерен катализатора, но и концентрациями веществ, участвующих в реакции. [34]
Скорость поглощения паров растворителя углем зависит в основном от продолжительности перемещения паров из пространства между каналами зерен угля до внутренней поверхности зерен. [35]
Поэтому каталитическая реакция протекает главным образом внутри зерен катализатора и обеспечивается диффузией реагентов сначала к внешней, а затем к внутренней поверхности зерен вдоль пор. По мере проникновения в глубь зерна ре-агенты расходуются в реакциях на стенке поры, поэтому необходимо использовать модель внутренней задачи. [36]
Если скорость химической реакции настолько мала, что скорость процесса не ограничивается переносом вещества ни к внешней, ни к внутренней поверхности зерна, и концентрации реагентов в газовой фазе на поверхности зерна и в центре его приблизительно равны, то процесс проходит в кинетической области. Закономерности такого процесса определяются закономерностями химического превращения, протекающего на активной поверхности катализатора. [37]
Поэтому каталитическая реакция протекает главным образом внутри зерен катализатора и обеспечивается диффузией реагентов сначала к внешней, а затем к внутренней поверхности зерен вдоль пор. По мере проникновения в глубь зерна реагенты расходуются в реакциях на стенке поры, поэтому необходимо использовать модель внутренней задачи. [38]
Если скорость химической реакции настолько мала, что скорость процесса совсем не ограничивается переносом вещества ни к внешней, ни к внутренней поверхности зерна, и концентрации реагентов в газовой фазе на поверхности зерна и в центре его приблизительно равны, то эти условия прохождения процесса называют кинетической областью. Закономерности такого процесса определяются закономерностями химического превращения, протекающего на активной поверхности катализатора. [39]
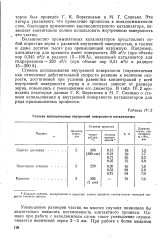 |
Степень использования внутренней поверхности катализатора. [40] |
Степень использования внутренней поверхности ( определяемая как отношение действительной скорости реакции к величине скорости, достигаемой при условии равенства концентраций у всей внутренней поверхности зерна и в потоке) зависит от размера зерна, повышаясь с уменьшением его диаметра. [41]
Эта модель удовлетворительно описывает процессы в адиабатическом слое катализатора при допущениях: градиенты температур внутри зерен катализатора незначительны; химические процессы на внутренней поверхности зерен и диффузионные процессы внутри пористых зерен квазистационарны по отношению к процессам переноса в газовой фазе; процессы межфазного тепло - и массообмена настолько интенсивны, что температура и концентрация реагента в твердой и газовой фазе неразличимы. [42]
В аппаратах КС идет одновременно отравление всей массы катализатора в данном слое, причем для яда доступна не только наружная, но и вся внутренняя поверхность зерна ввиду его малого размера. [43]
Каталитическая активность твердых пористых катализаторов определяется как их химическим составом, так и пористой структурой, при которой подразумевают совокупность формы зерен, объема и размера пор и внутренней поверхности зерна. Активность катализатора пропорциональна поверхности, доступной для реагентов, но в тонкопористых катализаторах внутренняя поверхность может быть использована далеко не полностью из-за диффузионных торможений. [44]
В тех случаях, когда величина L, вычисленная по формуле ( II, 70), велика в сравнении с размером зерна катализатора, мы можем считать, что работает вся внутренняя поверхность зерна. В тех случаях, когда величина L сравнима с диаметром пор, работает только внешняя поверхность зерна. В каждом из этих случаев необходимо еще удостовериться, в какой мере может оказаться существенной диффузия в объеме. [45]
Страницы: 1 2 3 4