Удельная поверхность - силикагель
Cтраница 4
Нами изучена теплоемкость бензола, адсорбированного крупнопористым силикагелем КСК-2, в широком интервале низких температур при различных величинах адсорбции. Теплоемкость адсорбционной системы бензол - силикагель измерена при различных величинах заполнения поверхности и пор силикагеля. Для удобства величину адсорбции относили к емкости плотного монослоя, величина которой была определена из известной удельной поверхности силикагеля и вандерваальсовых размеров молекулы бензола. [46]
Структура пор катализатора, а следовательно, и величина его удельной поверхности формируется на разных этапах приготовления катализатора и различным путем, в зависимости от типа катализатора. Для распространенных гелевых катализаторов и носителей регулирование структуры пор осуществляется либо на стадиях осаждения, промывки и прокалки, либо путем специальной гидротермальной обработки. Установлено [36, 37], что увеличению пористости сили-кагеля способствует рН 7 при осаждении и щелочная реакция промывных вод. Этими же работами установлено, что повышение температуры прокаливания свыше 600 С приводит к уменьшению удельной поверхности силикагеля и сокращению диаметра пор. Варьирование условий осаждения в отношении рН растворов, их концентрации, скорости осаждения и времейи вызревания осадков, а также температуры осаждения дает возможность путем изменения величины кристаллитов изменять пористость катализаторов / получаемых из кристаллических осадков. Исследованиями Кагановой с соавторами [41] показано для силикагелей и алюмоси-ликагелей, что наблюдаемые зависимости пористости готового катализатора от рН среды, температуры сушки, а также содержания окиси алюминия сводятся к взаимосвязи пористой структуры геля со степенью его синерезиса. [47]
Аэрогели показывали структуру кварца, а ксеро-гели - структуру тридимита, но оба вида аморфного кремнезема при температуре выше 600 - 800 С показывали изменения с образованием связей, характерных для кристобалита. На температуру, при которой удельная поверхность быстро падала до нуля, оказывали заметное влияние даже следы щелочных примесей. Удельная поверхность коммерческого силикагеля падала до нуля при температуре около 1040 С, а для аэрогеля, для которого было известно, что он приготовлялся по способу, предусматривающему включение сульфата натрия, удельная поверхность оказывалась равной нулю при 900 С. [48]
Гидротермальное старение силикагеля обусловлено стремлением системы к минимуму энергии Гиббса за счет уменьшения величины поверхности. Движущая сила релаксации связана здесь с зависимостью химического потенциала поверхности от ее кривизны. Вследствие этого в гидротермальных условиях растворяются мелкие глобулы скелета силикагеля, кремнезем осаждается на поверхности крупных глобул и в местах контакта глобул, куда переносится также кремнезем в результате поверхностной самодиффузии. Диаметр глобул при этом увеличивается, а удельная поверхность силикагеля уменьшается. [49]
В результате образуются глобулы, поверхность которых состоит из гидроксильных групп. Естественно, в местах контакта глобул благодаря той же реакции конденсации ( 2) возникают кислородные мостики Si - О - Si, прочно связывающие глобулы друг с другом. При этом вступает во взаимодействие лишь сравнительно небольшая часть гидроксильных групп. Таким образом возникает глобулярная структура силикагеля, обусловливающая его пористость и развитие удельной поверхности силикагеля. [50]
По данным [103] длительность активной работы фосфатных катализаторов не превышает нескольких часов. В связи с этим при осуществлении процесса в промышленности предполагается использовать реактор с псевдоожи-женным или движущимся слоем катализатора. В работе, проведенной И. И. Иоффе и авторами книги было установлено, что активность фосфатов кальция и кадмия лишь частично восстанавливается при регенерации, а гетерополикислоты ванадия, вольфрама и молибдена необратимо утрачивают активность после 4 - 6-часового рабочего цикла. В том случае, когда небольшие количества соляной кислоты пропускают вместе с потоком реагентов через слой силикагеля, последний сравнительно быстро изменяет свою структуру, в результате чего уменьшается активная поверхность носителя. Так, за 20 ч работы удельная поверхность силикагеля падает от 180 до 88 ма / г. Одновременно резко ухудшаются показатели процесса. В катали-зате методом ГЖХ обнаружены МВД, изоамиленовые спирты и небольшие количества ДМД. Однако указанные соединения содержатся в разбавленном водном растворе и превращение их в изопрен связано с большими трудностями. Кроме того, необходимость дополнительной переработки побочных продуктов в известной мере лишает рассматриваемый метод преимуществ одностадийного процесса. [51]
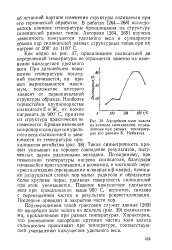 |
Адсорбция золя золота из ксилола силикагелей, прокаленным при разных температурах ( поданным Б. Неймана. [52] |
Как видно из рис. 37, прокаливание силикагелей до определенной температуры не отражается заметно на изменении кажущегося удельного веса. При дальнейшем повышении температуры последний увеличивается, на кривых вырисовывается максимум, положение которого зависит от первоначальной структуры образца. Наиболее термостойки крупнопористые силикагели Е и Ж, их можно нагревать до 900 С, при этом их структура практически не изменяется. Такая симметричность кривых указывает на хорошее совпадение результатов, полученных двумя различными методами. По-видимому, при повышении температуры нагрева силикагеля, благодаря начавшейся кристаллизации, а возможно, и частичной перекристаллизации ( превращении а-кварца вр-кварц), начинают разрушаться стенки пор малых радиусов и образуются более крупные поры; удельная поверхность силикагелей при этом уменьшается. Падение кажущегося удельного веса при прокаливании выше 950 С, вероятно, связано с перемещением частиц в результате рекристаллизации. Последнее приводит к закрытию части пор. [53]
Разделительная способность колонки зависит также от размеров отдельных частиц адсорбента. Обычно применяют активированный уголь с размером частиц 0 2 - 0 8 мм. Увеличение размеров частиц снижает разделительную способность колонки, так как при этом уменьшается суммарная активная поверхность адсорбента. Использование адсорбента с размером частиц меньше 0 2 мм не улучшает процесс разделения, а вызывает излишнее сопротивление колонки, которое в свою очередь ограничивает ее длину. Положительно на эффект разделения влияет однородность фракционного состава адсорбента. В колонках небольшого диаметра ( 3 - 5 мм) обычно применяют фракции угля 0 25 - 0 5 или 0 6 - 0 8 мм. К числу распространенных адсорбентов относятся сили-кагели, которые применяются в основном для разделения легких углеводородных газов, при этом непредельные углеводороды десорби-руются, как правило, позднее предельных. Силикагели различают по размеру пор: крупнозернистые - ШСК, МСК, КСК с удельной поверхностью 210 - 350 м / г и диаметром пор 12 - 15 нм, мелкопористые КСМ и ШСМ с удельной поверхностью 700 - 900 м / г и диаметром пор 1 - 2 нм и др. С уменьшением диаметра пор и увеличением удельной поверхности силикагелей разделение компонентов улучшается. [54]
Некоторые изотермы этого типа были изображены на рис. 7 для изученной Райер-соном и Камероном [18] адсорбции брома на силика-геле. Брунауер и Эммет [7.] измерили адсорбцию семи различных газов на двух образцах силикагеля, переданного им Райерсоном. Так как п относительно велико, то не будет серьезной ошибки, если положить п-оо и пользоваться при обработке данных Райерсона и Камерона простым уравнением ( 38), содержащим две константы. Другое упрощающее предположение касается константы с. Райерсон и Камерон вычислили по уравнению Клау-зиуса - Клапейрона [ гл. Это значение представляет, однако, теплоту адсорбции при образовании лишь части мономолекулярного слоя, и величина Е1 - средняя теплота адсорбции для всего первого слоя - может быть меньше этого значения. Если это верно, то из уравнения ( 38) следует, что vvm при / 0 5р0, и следовательно, константа vm может быть найдена из любой изотермы. Если вычислять величину поверхности, покрытой молекулами брома, исходя из плотности жидкого брома, то для удельной поверхности силикагеля получается значение 470л2 / з, что находится в превосходном согласии с величиной 500 м / г, найденной из изотерм типа / / для азота, аргона, кислорода, окиси углерода и сернистого газа, рассмотренных в предыдущем разделе. [55]
При е 1, или Е, EL уравнения ( 38) и ( 41) описывают изотермы типа III. Некоторые изотермы этого типа были изображены на рис. 7 для изученной Райер-соном и Камероном [18] адсорбции брома на еилика-геле. Брунауер и Эммет [7] измерили адсорбцию семи различных газов на двух образцах силикагеля, переданного им Райерсоном. Так как п относительно велико, то не будет серьезной ошибки, если положить поо и пользоваться при обработке данных Райерсона и Камерона простым уравнением ( 38), содержащим две константы. Другое упрощающее предположение касается константы с. Райерсон и Камерон вычислили по уравнению Клау-зиуса - Клапейрона [ гл. Это значение представляет, однако, теплоту адсорбции при образовании лишь части мономолекулярного слоя, и величина Ег - средняя теплота адсорбции для всего первого слоя - может быть меньше этого значения. Если это верно, то из уравнения ( 38) следует, что v - vm при р0 5р0, и следовательно, константа vm может быть найдена из любой изотермы. Если вычислять величину поверхности, покрытой молекулами брома, исходя из плотности жидкого брома, то для удельной поверхности силикагеля получается значение 470 л 2 / г, что находится в превосходном согласии с величиной 500 л 2 / г, найденной из изотерм типа / / для азота, аргона, кислорода, окиси углерода и сернистого га. [56]
Страницы: 1 2 3 4