Истинная поверхность - электрод
Cтраница 1
Истинная поверхность электродов, изготовленных из порошкообразных материалов, может во много раз превосходить их кажущуюся поверхность. [1]
Для определения истинной поверхности электрода емкость двойного слоя измеряют методом переменных токов. Этот метод используется в том случае, когда хотят определить истинную плотность тока при электроосаждении металлов. Однако здесь могут быть ошибки, заключающиеся в том, что из рассчитанной емкости получается общая величина поверхности, состоящая из растущих и нерастущих участков, поэтому рассчитанная плотность тока не соответствует истинной. [2]
Для определения истинной поверхности электрода емкость двойного слоя измеряют методом переменных токов. Этот метод используется в том случае, когда хотят определить истинную плотность тока при электроосаждении металлов. Однако здесь мргут быть ошибки, заключающиеся в том, что из рассчитанной емкости получается общая величина поверхности, состоящая из растущих и нерастущих участков, поэтому рассчитанная плотность тока не соответствует истинной. [3]
Плотность тока обратно пропорциональна истинной поверхности электрода, поэтому чем она меньше, тем выше плотность тока. Таким образом, именно на электродах с гладкой поверхностью создаются условия, благоприятные для поляризации катода до высокого отрицательного потенциала. [4]
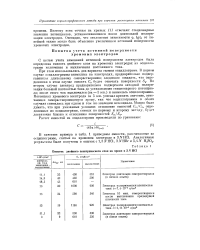 |
Емкость двойного электрического слоя на хроме в 3 TV HC1. [5] |
С целью учета изменений истинной поверхности электродов была определена емкость двойного слоя на хромовых электродах из осциллограмм включения и выключения постоянного тока. [6]
Принимая, что при постоянной истинной поверхности электрода S0 зависимость tp, lg / H линейна, нами были построены прямые IV, проводившиеся через точку саморастворения хрома и точки, отвечающие пересчитанным плотностям токов. [7]
Эта неопределенность в оценке значений истинной поверхности электрода еще более возрастает при электроосаждении или анодном растворении металлов, так как при этом поверхность электрода непрерывно меняется. [8]
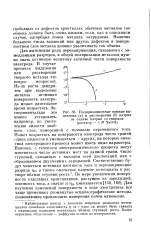 |
Поляризационные кривые выделения ( а и растворения ( б натрия на сплаве натрия со свинцом ( раствор - 1 N NaOH. [9] |
Из-за роста дендри-тов при выделении металла истинная поверхность электрода может длительное время возрастать. Экспериментально это можно установить, например, по увеличению емкости двойного слоя, измеренной с помощью переменного тока. Может возрастать на поверхности электрода число граней одних индексов и уменьшаться - других, на которых кинетика электродного процесса может иметь иные параметры. Наконец, с течением электрохимического процесса могут изменяться число активных мест на данной грани, число ступеней, связанных с выходом осей дислокаций или с образованием двухмерных зародышей. Для изучения изменений поверхности в ходе электролиза все чаще применяют упомянутые осциллографические методы, позволяющие производить измерения почти мгновенно. [10]
Очевидно, что в результате непрерывного изменения истинной поверхности электрода при электроосаждении металлов должна изменяться во времени и поляризация электродов. В некоторых случаях нестабильность поляризации электродов при постоянной плотности тока является следствием ряда сложных процессов, протекающих на электроде. Обычно для выяснения механизма электродных процессов изучают зависимость поляризации от плотности тока без учета того, что поляризация изменяется во времени. При этом для каждого значения плотности тока берут произвольные, в лучшем случае установившиеся значения поляризации. Исследователи, как правило, не учитывают то обстоятельство, что изменение поляризации в процессе электролиза характеризует изменение скоростей процессов, протекающих на электроде. Во многих случаях изучение изменения поляризации во времени значительно больше способствует проникновению в сущность электродных процессов, чем формальное определение зависимости поляризации от плотности тока. Одновременное исследование изменения поляризации и силы тока во времени, а также зависимости поляризации от плотности тока дает более полное представление об электродных процессах. [11]
Полагают также, что наряду с изменением величины истинной поверхности электрода не остается постоянной и ее активность. Указанные и некоторые другие затруднения, наблюдаемые при изучении г Ме, привели к заметной невоспроизводимости кривых потенциал - плотность тока, полученных различными исследователями. Можно привести примеры, когда даже одни и те же авторы прибегают к различным истолкованиям экспериментальных данных для объяснения природы явления перенапряжения на одинаковых металлических электродах. [12]
Если изменяется фактор шероховатости а, равный отношению истинной поверхности электрода к геометрической поверхности, то изменится предельная плотность тока и гомогенной реакции, которая поэтому все же будет зависеть от поверхности. [13]
Третьей причиной отличия формы реальной кривой от идеальной является изменение истинной поверхности электрода, связанное с характером подготовки поверхности. Увеличение поверхности должно вызывать смещение катодной кривой в область более положительных значений, а уменьшение, наоборот, в область более отрицательных. Для процессов с кислородной деполяризацией участок, характеризующий предельный диффузионный ток, может не изменяться при изменении истинной поверхности в связи с тем, что эффективность диффузионного процесса зависит не только от истинной поверхности катода, но и от габаритной поверхности поляризуемого электрода. [14]
Для определения емкости в расчете на 1 м2 необходимо знать истинную поверхность электрода. При определении поверхности платинового электрода можно воспользоваться методом БЭТ, который основан на низкотемпературной адсорбции инертного газа, а затем сопоставить найденную поверхность с величиной адсорбции водорода. При этом был получен приближенный вывод о том, что на каждом поверхностном атоме платины при обратимом водородном потенциале ( / 7н20, 1 МПа) адсорбирован один атом водорода. Поэтому, определяя по длине водородной области количество Надс при обратимом водородном потенциале в сернокислом растворе, можно легко рассчитать истинную поверхность исследуемого электрода. [15]
Страницы: 1 2 3 4