Повышение - концентрация - реагент
Cтраница 1
Повышение концентрации реагента в растворе способствует значительному повышению темпа вытеснения и уменьшению фазовой проницаемости породы. [1]
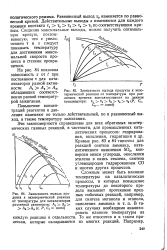 |
Зависимость выхода продукта х экзотермической реакции от температуры для катализаторов различной активности. Ах А2 А3 А4 ( t, Р, Ci - const. [2] |
Повышение концентраций реагентов и давления изменяют не только действительный, но и равновесный выход, а также температуру зажигания. [3]
Повышение концентрации реагентов обусловливает не только ускорение реакции, но и уменьшение объема аппаратуры, экономию транспорта и изменение ряда других техно-экономических показателей. [4]
Повышение концентрации реагентов в реакционной зоне совмещенного процесса способствует также увеличению избирательности химического процесса если имеются параллельные побочные реакции, так как в этом случае есть возможность достигнуть той же скорости основной реакции, что, например, и в простых проточных или периодических реакторах, но при более низкой температуре. Увеличение селективности процесса за счет этой дополнительной возможности будет тем больше, чем больше различие в температурных коэффициентах скорости основной и побочных реакций. [5]
Повышением концентрации реагентов С и давления Р до оптимальных значений увеличивают АС. Перемешивание приводит к увеличению k только в тех случаях, в которых медленно происходит диффузия реагентов в зону реакции. Температура - наиболее универсальное средство интенсификации технологических процессов; повышение ее ускоряет химические реакции и в меньшей степени диффузию. Однако повышение температуры ограничено термостойкостью материалов и приводит к уменьшению АС в обратимых экзотермических процессах. Таким образом, интенсифицирующее действие всех параметров технологического режима ограничено, за исключением действия катализаторов. [6]
При этом повышение концентрации реагента ( реагентов) сме -, щает равновесие в сторону образования - продуктов реакции. Наоборот, добавление продукта ( продуктов) реакции смещает равновесие в сторону образования реагентов. Таким образом, направление смещения равновесия определяется тем, концентрация какого из взаимодействующих веществ меняется: реагентов или продуктов реакции, а степень смещения - величиной изменения концентрации и стехиометрическими коэффициентами. [7]
Выход карбамида растет с повышением концентрации реагентов и с увеличением избытка МНз, препятствующего образованию побочных продуктов. [8]
Повышение давления ускоряет газовые реакции аналогично повышению концентрации реагентов, так как с ростом давления увеличиваются концентрации компонентов. Следовательно, влияние давления увеличивается с возрастанием порядка реакции. Особенно благоприятно применение давления для процессов, протекающих с уменьшением газового объема, так как в этом случае, согласно принципу Ле-Шателье, повышение давления вызывает увеличение выхода продукта. [9]
Повышение давления ускоряет газовые реакции аналогично повышению концентрации реагентов, так как с ростом давления увеличиваются концентрации компонентов. Следовательно, влияние давления увеличивается с возрастанием порядка реакции. [10]
Об этих ограничениях необходимо помнить при повышении концентрации реагентов. [11]
Иногда пульпу перед контактом с реагентами для повышения концентрации реагента приходится сгущать, а перед флотацией - разбавлять. [12]
Таким образом, в согласии с теорией повышение концентрации реагента приводит к возрастанию % инвертированного соединения и к падению % рацемизованного соединения. [13]
Таким образом, в согласии с теорией повышение концентрации реагента приводит к возрастанию процента инвертированного соединения и к падению процента рацемизованного соединения. [14]
Как видно, предельная плотность тока может быть увеличена путем повышения концентрации реагентов. [15]
Страницы: 1 2 3 4