Повышение - концентрация - реагент
Cтраница 2
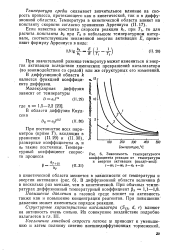 |
Зависимость температурного. [16] |
Повышение давления в газовой среде влияет на активность также как и повышение концентрации реагентов. При повышении давления может измениться порядок реакции. [17]
Повышение давления влияет на скорость химического процесса не только в результате повышения концентрации реагентов, но и вследствие изменения константы скорости реакции. Однако увеличение константы скорости становится заметным лишь при очень высоких давлениях - порядка тысяч и десятков тысяч атмосфер. [18]
Суммарные выходы продуктов алкилирования составляют - 50 90 % и возрастают при повышении концентрации реагентов, переходе от литиевых солей дианиона 22 - к калиевым, от алкилх-лоридов к бромидам и иодидам, от третичных к первичным алкил-галогенидам, и с уменьшением длины алкильной цепи. Зависимость от природы противоиона может быть связана с большей основностью литиевых и натриевых солей дианиона 22 - по сравнению с калиевыми, поскольку в реакциях солей первых двух катионов довольно значительно образование бензонитрила ( до 10 %), причиной которого, очевидно, является протонирование дианиона 22 - продуктами аммонолиза алкилгалогенида или следами влаги. [19]
Увеличение давления в газовой среде влияет на активность так же, как и повышение концентрации реагентов. При возрастании давления может измениться порядок реакции. [20]
Под воздействием гравитационных сил и конвективной циркуляции аэрозоли перемещаются, вызывая в отдельных зонах повышение концентрации реагента. [21]
Рекомбинация атомов и очень простых радикалов в газовой фазе часто требует участия третьей частицы, поэтому повышение концентрации реагентов или инертного газа будет вызывать увеличение скорости. Активация за счет столкновений, приводящая к распаду простых радикалов, таких, как ОН, СЮ и HGO, по-видимому, является реакцией второго порядка даже при обычно используемых давлениях. [22]
Переход процесса во внешнедиффузионную область может произойти при уменьшении линейной скорости потока и размера зерна катализатора, повышении концентраций реагентов и особенно при повышении температуры. [23]
Обобщая сказанное, приходим к выводу, что при более высоком порядке основной реакции по сравнению с побочной повышение концентрации реагента будет способствовать росту выхода. И наоборот, если основная реакция имеет более низкий порядок, то выход растет с понижением этой концентрации, в результате чего может быть скомпенсировано соответствующее уменьшение скорости реакции. [24]
 |
Выбор оптимального РСНД с заданным числом ступеней в случае проведения параллельных реакций. [25] |
Обобщая сказанное, приходим к выводу, что при более высоком порядке основной реакции, по сравнению с побочной, повышение концентрации реагента будет способствовать росту выхода продукта. И, наоборот, если основная реакция имеет более низкий порядок, то выход растет с понижением этой концентрации, в результате чего может быть скомпенсировано соответствующее уменьшение скорости реакции. [26]
Дополнительное введение в разбавленный раствор реагента сравнительно больших количеств электролитов ( например, 0 5 М NaCl) производит такое же действие, как повышение концентрации реагента. [27]
При проведении поликонденсации бензила и гидразингидрата в среде масляной кислоты при 140 С с отгонкой водного азеотропа получают полиазины с М 2200, причем повышение концентрации реагентов выше 10 % не приводит к увеличению молекулярного веса полимера. [28]
Дополнительное введение в разбавленный раствор реагента сравнительно больших количеств электролитов ( например, 0 5 М NaCl) производит такое же действие, как повышение концентрации реагента. [29]
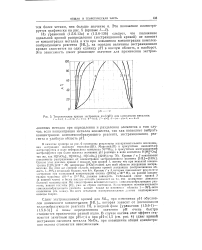 |
Теоретические кривые экстракции pf ( pH для комплексов MI. [30] |
Страницы: 1 2 3 4