Повышение - концентрация - реагирующее вещество
Cтраница 2
Как известно, скорость химических реакций растет при повышении концентрации реагирующих веществ, увеличении площади их соприкосновения и температуры. [16]
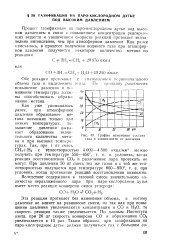 |
График изменения cocraua газа в зависимости от давления. [17] |
Процесс газификации на паро-кислородном дутье под высоким давлением в связи с повышением концентрации реагирующих веществ и увеличением скорости реакций протекает значительно интенсивнее, чем при атмосферном давлении. [18]
Мартин с сотрудниками нашел, что скорость реакции заметно возрастает с повышением концентрации реагирующих веществ. При сравнимых концентрациях наблюдается большое повышение активности смешанного катализатора по прибавлении хлорного железа. Хлористый алюминий Гульф рифайнинг компапи был значительно более активен, чем можно было ожидать по содержанию в нем хлорного железа; его более высокая активность, невидимому, зависит частично от содержания в нем хлористого титана. [19]
Объясните ( с точки зрения молекулярной теории), почему при повышении концентрации реагирующих веществ может увеличиваться скорость реакции. [20]
Итак, интенсификация процессов горения и газификации в условиях диффузионной области, помимо повышения концентраций реагирующих веществ, возможна путем увеличения линейной скорости газов и уменьшения размера частиц твердого топлива. [21]
Фарадей высказал предположение, что каталитическое ускорение реакции достигается благодаря адсорбционному сгущению - повышению концентрации реагирующих веществ в зоне реакции - адсорбционном слое и увеличению благодаря этому числа столкновений. Однако такая трактовка недостаточна, так как она может объяснить ускорение реакции не более чем в 102 ч - 10 раз, в то время как, например, реакция Н2 - - О а ускоряется даже на фарфоре - сравнительно инертном катализаторе - в 107 ч - 108 раз. [22]
Химики установили, что во многих случаях, хотя и не всегда, при повышении концентрации реагирующих веществ скорость реакции возрастает. В этом разделе мы разберем, почему возрастает скорость реакции с повышением концентрации реагирующих веществ. В разделе 8 - 1.3 мы изучим вопрос, почему скорость некоторых реакций не зависит от концентрации одного или нескольких реагирующих веществ. Оба объяснения основаны на моделировании химических реакций с помощью молекулярных моделей. [23]
Большое значение для увеличения скорости передела имеет обогащение воздуха кислородом или полная замена воздуха кислородом вследствие повышения концентрации реагирующих веществ и одновременного повышения температуры. [24]
Когда было установлено значение адсорбционных явлений в гетерогенном катализе, возникло предположение, что каталитическая активность обусловливается повышением концентрации реагирующих веществ на поверхности раздела фаз. Более глубокое изучение этого явления показало, что в каталитическом действии основную роль играет адсорбция реагирующих веществ на наиболее активных центрах поверхности. При этом определенное значение имеют химические взаимодействия, сопровождающиеся изменением свойств адсорбируемых молекул. Что касается природы активных центров, то она изучалась многими исследователями. В итоге было выдвинуто несколько теорий. Основными из них являются мультиплетная теория, теория активных ансамблей и электронная теория. [25]
Общим свойством всех органических и неорганических преобразователей химической энергии является то, что на их поверхности вследствие адсорбции происходит повышение концентрации реагирующих веществ и что сравнительно инертный кислород не реагирует непосредственно с веществом, подлежащим окислению. В живом организме кислород соединяется с железом гемоглобина и образует при этом перекисное соединение, окисляющее субстрат в качестве переносчика кислорода. Аналогично активируется весьма инертный при комнатной температуре кислород на диффузионных катодах соответствующими переносчиками вроде дисперсного серебра или металлической платины. [26]
Когда было установлено значение адсорбционных явлений для активности катализатора, то в первое время высказывались предположения, что каталитическая активность обусловливается повышением концентрации реагирующих веществ, поглощаемых катализатором. Подобное повышение концентрации может влиять на скорость реакции, но им никак нельзя объяснить нередко наблюдаемую на опыте очень высокую активность катализатора и высокую специфичность катализирующего действия. В некоторых реакциях гетерогенного катализа скорость реакции возрастает чрезвычайно резко ( иногда от практически нулевой скорости); это указывает на очень сильное снижение энергии активации и не может быть объяснено только повышением концентрации. [27]
Когда было установлено значение адсорбционных явлений для активности катализатора, то в первое время высказывались предположения, что каталитическая активность обусловливается повышением концентрации реагирующих веществ, поглощаемых катализатором. Подобное повышение концентрации может влиять на скорость реакции, но им никак нельзя объяснить нередко наблюдаемую на опыте очень высокую активность катализатора и высокую специфичность катализирующего действия. [28]
Анализируя уравнения ( 39) - ( 53), можно видеть, что чем выше порядок реакции, тем больше она ускоряется с повышением концентрации реагирующих веществ. [29]
Однако необходимо отметить, что переход органических молекул в водную фазу ( всаливание) может привести в конечном итоге к так называемому мицеллярному катализу вследствие образования мицелл под действием поверхностно-активных веществ и повышения концентрации реагирующих веществ внутри мицеллы. Эту возможность следует учитывать, поскольку многие ониевые соли являются поверхностно-активными веществами. В том случае, когда в молекуле ониевой соли имеется одна или две длинноцепочечные группы, мицеллообра-зование наступает довольно быстро. [30]
Страницы: 1 2 3 4