Повышение - основность
Cтраница 3
Для повышения срока службы футеровки миксера необходимы обеспечение стабильного количества чугуна, повышение основности шлака, возможное его уменьшение за счет скачивания, внедрение постоянного торкретирования, в первую очередь шлакового пояса и углов сливного носка. [31]
При Y - С1 - скорости реакций уменьшаются при повышении основности амина ( повышение основности, вероятно, симбатно увеличению прочности связи Аи - N) BTO время как при Y - NOJT или N - наблюдается увеличение скоростей реакций для той же серии комплексов. Эти результаты легко могут быть объяснены. Это значит, что в образование ПС существенный вклад вносит разрыв связи А - N и, следовательно, с ростом основности амина реализация этого состояния становится более трудной из-за повышения прочности связи. Первоначальное повышение скорости с повышением основности амина позволяет предположить, что входящая группа с большей легкостью образует связь в ПС А. [32]
CaO MgO) / SiO2s: 0 15 -: - 0 20i Повышение основности шлака нежелательно, так как способствует увеличению восстановления марганца в попутный сплав и ухудшает условия дефосфорации шлака. Выпуск шлака производится два-три раза в смену в стальные нефутерованные ковши и один раз в двое суток выпускают в ошлакованный ковш образующийся железомарганцевый сплав ( попутный металл), содержащий 52 - 62 % Мщ 28 - 37 % Fe, 3 0 - 6 0 % С, 0 5 - 2 7 % Si и 2 5 - 4 0 % Р, который находит применение при выплавке автоматной стали; количество его невелико: 50 - 70 кг на 1 т шлака. [33]
При таком толковании механизма активирующего действия воды следует ожидать ослабления этого действия с повышением основности носителя катализатора. Это действительно имеет место, когда в качестве носителя используется вместо СгоОз окись алюминия. Так, в случае гидрирования АДН на катализаторе Ni - А1203 активирующего действия воды вовсе ие наблюдается. [34]
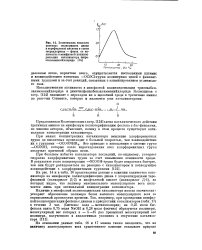 |
Зависимость вязкости раствора полиарилата диана и терефталевой кислоты в смеси тетрахлорэтан - фенол от количества в межфазной поликонденсации катализатора тетра-этиламмонийхлорида. [35] |
При большом избытке катализатора последний, по-видимому, ускоряет гидролиз хлорформиатных групп за счет повышения основности среды. [36]
Небольшой индуктивный эффект, вызываемый обычно ме-гильными группами, хотя и может привести к некоторому повышению основности, однако он не достаточен для того, чтобы заметно дестабилизировать катион; важную роль играют здесь также стерические факторы и возможные изменения сольватации. Группа, обусловливающая более мощный индуктивный эффект ( например, NO2), оказывает гораздо бол ее сильное влияние. Этот эффект усиливается, если нитрогруппа находится. [37]
Небольшой индуктивный эффект, вызываемый обычно ме-гильными группами, хотя и может привести к некоторому повышению основности, однако он не достаточен для того, чтобы заметно дестабилизировать катион; важную роль играют здесь также стерические факторы и возможные изменения сольватации. Группа, обусловливающая более мощный индуктивный эффект ( например, NO2), оказывает гораздо более сильное влияние. Этот эффект усиливается, если нитрогруппа находится. [38]
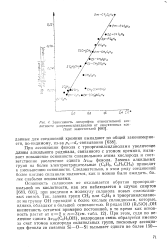 |
Зависимость логарифма относительной кислотности диорганосиландиолов от индуктивных констант заместителей. [39] |
При ассоциации фенола с триорганилсиланолами увеличение длины алкильного радикала, связанного с атомом кремния, вызывает повышение основности силанольного атома кислорода и соответственно увеличение сдвига AVOH фенола. Замена алкильных групп на более электроотрицательные ( C6Hs, C6H5CH2) приводит к уменьшению основности. Следовательно, в этом ряду соединений более кислые силанолы являются, как и можно было ожидать, более слабыми основаниями. [40]
Приведенные на рис. 4.10 зависимости показывают рост содержания кокса на цирконийалюмосиликатном катализаторе ( температура крекинга 500 С) с повышением основности и фиктивного времени реагирования крекируемого ароматического углеводорода. Основность ароматических углеводородов, по-видимому, отражает склонность к хемосорбции на поверхности и влияет аналогично фиктивному времени реагирования. [41]
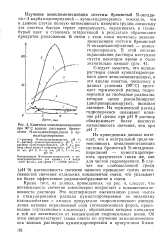 |
Кинетика хемилюминесценции при 90 С водных растворов бромистого N-октадецилпиридиния и ку-милгидроперекиси. [42] |
Кроме того, из данных, приведенных на рис. 4, следует, что интенсивность свечения закономерно возрастает с повышением основности раствора. Это подтверждает высказанную ранее мысль о стимулировании распада кумилгидроперекиси по механизму взаимодействия с амином продуктами гидролитического расщепления катиона пиридиниевой соли ( псевдоосновная форма, производное глутаконового альдегида), образование которых находится в той же зависимости от концентрации гидроксильных ионов. [43]
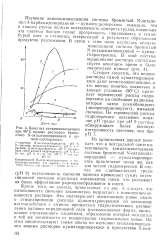 |
Кинетика хемилюминесценцйи при 90 С водных растворов бромистого N-октадецилпиридиния и ку-мил гидроперекиси. [44] |
Кроме того, из данных, приведенных на рис. 4, следует, что интенсивность свечения закономерно возрастает с повышением основности раствора. Это подтверждает высказанную ранее мысль о стимулировании распада кумилгидроперекиси по механизму взаимодействия с амином продуктами гидролитического расщепления катиона пиридиниевон соли ( псевдоосновная форма, производное глутаконового альдегида), образование которых находится в той же зависимости от концентрации гндроксильных ионов. [45]
Страницы: 1 2 3 4