Повышение - полярность - растворитель
Cтраница 1
Повышение полярности растворителя вызывает обычно гипсохромный сдвиг п - - л - переходов [ 7а ] и батохромный сдвиг л - - л - переходов. [1]
С повышением полярности растворителя в растворе появляются значительные количества пиридониминной формы, причем в большинстве растворителей ее содержание меньше для фенилртутного производного, чем для незамещенного соединения. [3]
Скорость реакции снижается с повышением полярности растворителя в соответствии с теорией Гюйгеса - Инголда. Ион сульфита в реакциях этого типа более нуклеофилен, чем алкокспд. [4]
Оказалось, что с повышением полярности растворителя растет скорость образования мстилен-бисфеполов и затрудняется выделение целевого 4-гидрокси - 3 5-ди-трег - бутилбснзиловоп) спирта [152]: с такими растворителями, как метанол, этанол или изопроианол, последний взаимодействует с образованием соответствующих эфиров. Лучшие результаты получены с применением безводного грет-бутапола. Выход целевого продукта подрастает, если в качестве агента оксимстилировання1 использовать параформ. [5]
Поэтому обе реакции при повышении полярности растворителя должны быть замедлены. Но так как в реакции Е2 заряд делокализуется в большей степени ( распределяется по большей части молекулы), чем в Sjv2, то увеличение полярности растворителя должно сильнее тормозить элиминирование, чем замещение. В связи с этим при реакции какого-либо алкилгалогенида с гидроксильным или алкоксильным анионом выход олефина должен уменьшаться при увеличении полярности растворителя. [6]
Обе реакции замедляются при повышении полярности растворителя. [7]
Данные о том, что повышение полярности растворителя не увеличивает скорость замещения, являются косвенным доказательством того, что ионные заряды не возникают и не исчезают в стадии, определяющей скорость реакции. В случае бромирования приведенный механизм реакций совместим с этим положением, а также с данными, излагаемыми ниже. [8]
Полученные в наших исследованиях результаты отчетливо показывают, что с повышением полярности растворителей понижается степень ассоциации асфальтенов и смол в растворах. Отрицательно влияет ла ассоциацию асфальтенов и смол в растворах и повышение температуры. [9]
Полученные и наших исследованиях результаты отчетливо показывают, что с повышением полярности растворителей понижается степень ассоциации асфальтепов и смол в растворах. Отрицательно влияет на ассоциацию асфальте по и смол в растворах и повышение температуры. [10]
Полученные в наших исследованиях результаты отчетливо показывают, что с повышением полярности растворителей понижается степень ассоциации асфальтенов и смол в растворах. Отрицательно влияет на ассоциацию асфальтенов и смол в растворах и повышение температуры. [11]
 |
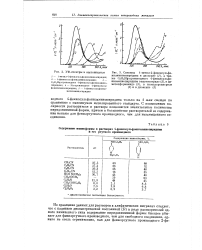
Влияние различных растворителей на электронный спектр ( CH3 2N - N0. У-вода. г-этанол. а-диоксан. 4 - цвклогексан. [12] |
Для полос поглощения, обусловленных я - я - переходом, повышение полярности растворителя обычно приводит к батохромнбму эффекту, тогда как при уменьшении полярности растворителя лри я - - - я наблюдается гипсохром-ный эффект. [13]
Далее, было установлено, что полярность флуоресцентного состояния с переносом заряда увеличивается при повышении полярности растворителя, поскольку при этом увеличивается время жизни флуоресцентного состояния с переносом заряда ту, а его квантовый выход t j уменьшается с повышением полярности растворителя. [14]
Тот факт, что подобная ионизация лимитирует скорость процесса, подтверждается также возрастанием скорости реакции с повышением полярности растворителя. [15]
Страницы: 1 2 3