Повышение - энергия - активация
Cтраница 1
Повышение энергии активации с ростом размеров частиц является интересной особенностью процесса. [1]
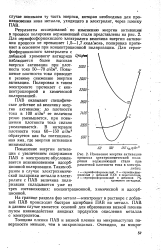 |
Изменение энергии активации процесса электрохимической полировки нер жавеющей стали прю различной плотности тока в электро. [2] |
Повышение энергии активации с увеличением содержания ПАВ в электролите обусловливается возникновением адсорбционной поляризации. [3]
Следовательно, причиной повышения энергии активации полиэтилена низкой плотности является наличие в полимере более длинных боковых цепей, чем этильные. [4]
С этих же позиций объясняется повышение энергии активации самодиффузии железа при добавлении хрома. [5]
Увеличение степени ассоциации приводит к повышению энергии активации вязкого течения. [6]
Область пассивных составов обычно связывают с повышением энергии активации перехода ионов металла из решетки сплава в раствор ( из-за влияния адсорбата), как это следует из типично выраженной анодной поляризации многих металлов в пассивирующей среде. Недавно Бонд в нашей лаборатории показал, что анодная поляризация сплавов Си - Ni в растворе Na2SO4 претерпевает заметное изменение в интервале состава, приблизительно соответствующего заполнению d - зопы, причем значения поляризации оказываются более высокими для сплавов с - электронными вакансиями. Описаны [24, 25] и каталитические свойства, зависящие от электронных конфигураций в Си - Ni - и других сплавах с аналогичными конфигурациями, оказывающими влияние на скорость коррозии. [7]
Увеличение числа химических связей между макромолекулами сопровождается повышением энергии активации диффузии. [8]
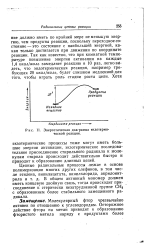 |
Энергетическая диаграмма эндотермической реакции. [9] |
Так как известно, что при комнатной температуре повышение энергии активации на каждые 1 4 ккал / моль замедляет реакцию в 10 раз, легко видеть, что эндотермическая реакция, например требующая 20 ккал / моль, будет слишком медленной для того, чтобы играть роль стадии роста цепи. [10]
Для вытеснения лиганда требуется дополнительная энергия, что вызывает повышение энергии активации. Такое предположение подтверждается фактом уменьшения скорости реакции и увеличения энергии активации при переходе от протонных растворителей к апротонным. [11]
При температурах ниже 650 С начинается постепенная сульфатизация и повышение энергии активации до 280 кдж / молъ. [12]
Ускоряющий эффект акцепторных заместителей, сопровождающийся не понижением, а повышением энергии активации, не представляется возможным интерпретировать в рамках электронной стабилизации переходного состояния этими заместителями. [13]
Адсорбция катионов приводит к изменению строения двойного слоя, которое влечет за собой повышение энергии активации катодной реакции. На это указывает уменьшение скорости ее, наблюдаемое при изучении кинетики. Но такое влияние адсорбции может быть выражено в большей или меньшей степени. [14]
Первым следствием этого является увеличение притяжения между Y и Z, что приводит к повышению энергии активации и к уменьшению скорости реакции; с другой стороны, увеличение притяжения между X и Y приводит к уменьшению энергии и увеличению скорости. Эти два эффекта поэтому действуют в противоположных направлениях. В большинстве изученных Sjy2 реакций влияние заместителей в YZ определяется действием второго эффекта; другими словами, наиболее важным является взаимодействие между реагирующими молекулами. Таким образом, влияние заместителя в каждом случае противоположно тому, что наблюдается при механизме S. Возможны, однако, реакции 5дг2, в которых влияние заместителей приближается к их влиянию на реакции S / Л; это обнаруживается в тех случаях, когда связь Y - Z сама по себе значительно ионизирована в переходном состоянии. [15]
Страницы: 1 2 3 4