Поглощение - окись
Cтраница 2
Значение энергии активации поглощения окиси азота реагирующей системой дифениламин - перекись бензоила указывает па то, что первичным актом зарождения цепи является реакция между валентно насыщенными молекулами дифениламина и перекиси. [16]
Получены инфракрасные спектры поглощения окиси азота, адсорбированной на железе, никеле, хроме и их сульфатах, нанесенных на алюмогель, а также на Fe2O3 -, Сг203 - гелях и порошке NiO. Наблюденные колебательные спектры могут быть приписаны различным валентным состояниям молекул NO, взаимодействующим с разного рода адсорбционными центрами поверхности. [17]
На рисунке представлены ИК-спектры поглощения окиси цинка и адсорбированного на ней этанола при различных температурах. Для сравнения на этом же рисунке приведен спектр газообразного этанола. При сопоставлении этих спектров с учетом собственного поглощения окиси цинка можно видеть существенное различие, появляющееся в результате адсорбции молекул С2Н5ОН на окиси цинка. Адсорбция этанола при 20 С с откачкой в течение часа ( кривая 3) приводит к появлению в спектре интенсивных полос в области 1100 - 800 см-1 с максимумами 1090 и 1050 см-1 и слабого поглощения около 1390 см-1. Газообразный этанол имеет интенсивную полосу 1080 ел - 1, которую обычно приписывают валентному колебанию С-С - О и деформационному колебанию связи ОН. [18]
Это определение основано на поглощении окиси этилена подходящим раствором или твердым адсорбентом. [19]
Было установлено, что на полноту поглощения окиси этилена большое влияние оказывает концентрация кислоты, а не высота столба жидкости, через которую проходит воздух. [20]
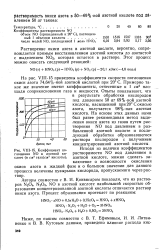 |
Коэффициент поглощения NO в азотной кислоте ( в см3 газа / ел3 кислоты. [21] |
На рис. VIII-15 приведены коэффициенты скорости поглощения окиси азота 74 64 % - ной азотной кислотой при 20 С. Примерно такое же значение имеют коэффициенты, отнесенные к 1 см2 площади соприкосновения газа и жидкости. [22]
Нашими опытами установлено, что скорость поглощения окиси азота реагирующей системой возрастает при повышении концентраций как дифениламина, так и перекиси бензоила. Хотя эти данные в условиях наших опытов но строго воспроизводимы, но наблюдаемая зависимость скорости поглощения окиси азота близка к пропорциональности последней корню квадратному из концентраций как амина, так и перекиси. [23]
На рис. 122 приведены коэффициенты скорости поглощения окиси азота 74 64 % - ной азотной кислотой при 20, выраженные в см3 газа, поглощенного 1 см3 кислоты. Примерно такое же значение имеют коэффициенты, отнесенные к 1 см2 площади соприкосновения газа и жидкости. [24]
Из данных предварительных опытов определения температурной зависимости скорости поглощения окиси азота реагирующей системой перекись бензоила - дифениламин в ацетоновом растворе было оценено значение энергии активации этого процесса, равное 12 4 8 ккал / моль. [25]
Ленсовета опытами было установлено, что в пенном контакте Еаз происходит поглощение окиси азота из газа, содержащего кис-юрод ( без предварительного окисления NO), щелочными поглоти - елями без добавки к ним окислителей. Степень абсорбции NO на вдной полке пенного аппарата составляет примерно 10 %, независимо от начальной нитрозности газа. Эти 1анные говорят о том, что при пенном режиме взаимодействия фаз вдет значительное окисление NO в жидкой фазе ( см. стр. [26]
Приведенные шесть условий могут быть выражены алгебраически через известные коэфициенты окисления NO, поглощения окиси, испарения НаО и теплопереноса, и через энтальпии веществ, участвующих в происходящих процессах. Эти условия могут быть-преобразованы в желаемые дифференциальные уравнения, которые можно проинтегрировать и получить численный результат, выразив V через h и продифференцировав. [27]
Концентрированный раствор сульфата железа ( II), подкисленный серной кислотой, - для поглощения окиси азота. [28]
Идентификация свободного радикала дифенилазота возможна двояким пухом: цветной реакцией с серной кислотой и поглощением окиси азота. [29]
Возникновение свободного радикала дифенилазота в результате взаимодействия дифениламина с перекисью бензоила нами установлено также поглощением окиси азота реагирующей системой. Однако при смешении этих растворов ( в погруженной и термостат колбе с двумя сообщающимися отделениями, соединенной с газовой бюреткой, наполненной окисью азота) сейчас же начинается быстрое поглощение окиси азота реагирующей системой. Само собой разумеется, что до смешения растворы замораживались, многократно откачивались и промывались чистым азотом и затем только приводились л соприкосновение с окисью азота. Растворы с реагентами смешивались друг с другом после того, как в течение 1 часа не наблюдалось сколько-нибудь заметного изменения объема газа в газовой бюретке при постоянной температуре реактора и бюретки. [30]
Страницы: 1 2 3 4