Закись - марганец
Cтраница 1
Закись марганца определяется только в том случае, если она содержится в сырьевых материалах. Обычно закись марганца определяют в огнеупорных материалах колориметрически. [1]
Закись марганца МпО - основной окисел серо-зеленого цвета, пл1785, на воздухе окисляется, при растворении в кислотах образует соли двухвалентного марганца слабо-розовой окраски. [2]
Закись марганца МпО имеет основной характер, она пол чается прокаливанием Мп ( ОН) 2, МпСО3, МпС2О4 и некоторы других соединений без доступа воздуха. [3]
Закись марганца МпО может быть получена нагреванием пиролюзита в струе водорода. Представляет собой зеленый порошок, нерастворимый в воде, но легко растворяющийся в кислотах с образованием солей двухвалентного марганца. [4]
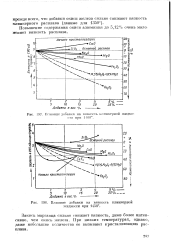 |
Влияние добавки на вязкость клинкерной жидкости при I lOO.| Влияние добавки на вязкость клинкерной жидкости при 1450. [5] |
Закись марганца сильно снижает вязкость, даже более интенсивно, чем окись железа. [6]
Закись марганца МпО может быть получена восстановлением высших окислов или прокаливанием карбоната марганца МпСОа в отсутствие кислорода. На воздухе она сгорает и превращается в высшие окислы. [7]
Закись марганца МпО образуется при прокаливании Мп ( ОН) г, МпСОя или МпСгО4 без доступа воздуха или же при прокаливании другого какого-нибудь окисла марганца в токе водорода. Она представляет собой серый или зеленовато-серый порошок, окисляющийся на воздухе в Mn. Гидрозакись марганца Мп ( ОН) 2 образуется при действии едкой щелочи на соли двухвалентного ма рга ца. [8]
Закись марганца МпО получается из двуокиси марганца МпО2 или закись-окиси Мп3О4 восстановлением водородом при 400 - 500 С. Между тем даже тщательно осушенный водород содержит влаги больше, чем это соответствует константе равновесия реакции окисления металла до закиси. [9]
Закись марганца растворима в аммонийных солях, что обусловливает равновесие реакции. Очевидно, в присутствии аммонийной соли осаждения не произойдет. Вследствие этого при обработке аммиаком кислого раствора или раствора, содержащего аммонийную соль, марганец может оказаться и в растворе и в осадке. [10]
Закись марганца в большей своей части переходит в шлак. [11]
Закись марганца в большей своей части переходит в шлак. [12]
Закись марганца ( МпО) легко реагирует с кислыми окислами. С кремнеземом образует силикат марганца MnO SiO2, переходящий в шлаки, а с закисью железа - ряд растворов в жидком и твердом состоянии. [13]
Закись марганца МпО образуется при прокаливании Мп ( ОН) г, МпСОя или МпСгО4 без доступа воздуха или же при прокаливании другого какого-нибудь окисла марганца в токе водорода. Она представляет собой серый или зеленовато-серый порошок, окисляющийся на воздухе в Mn. Гидрозакись марганца Мп ( ОН) 2 образуется при действии едкой щелочи на соли двухвалентного марганца. [14]
Закиси марганца соответствует Мп ( ОН) 2 - гидрат закиси марганца; белый осадок, быстро темнеющий на воздухе, вследствие окисления марганца до трехвалентного состояния: Мп ( ОН) 2 постепенно переходит в гидрат окиси Мп ( ОН) 3 темного цвета. [15]
Страницы: 1 2 3 4