Подвижность - кислород
Cтраница 1
Подвижность кислорода в решетке окислов в последнее время часто оценивается по скорости изотопного обмена твердого тела с газом. Работы Винтера и сотрудников [ 1J, Г. К. Борескова и Л. А. Касаткиной [2], С. М. Карпачевой и А. М. Розена [3] показали, что кинетика обмена имеет диффузионный характер; определяющей стадией обмена является степень подвижности кислорода в решетке окисла. Одной из существенных особенностей современных представлений в химии и физике полупроводников является представление о так называемых структурно чувствительных свойствах твердых тел. К таким свойствам относятся электропроводность, работа выхода и ряд других параметров, зависящих от предыстории твердого тела и его химического состава. Учение о полупроводниковых свойствах прежде всего основывается на картине реальной решетки с учетом локальных нарушений строго периодической структуры и отклонений от стехио-метрического состава. Эти нарушения в физике полупроводников могут быть охарактеризованы как при помощи метода электропроводности, так и другими способами. Большинство известных систем окислов-полупроводников ( Cu20, NiO, ZnO, Cr203, V20 - и др.) имеет нестехиометриче-ский состав. Естественно, что особенности химического и электронного состояния твердого тела должны определять подвижность ионов металла и металлоида и тем самым влиять на обмен между твердым телом и газом. Методы изучения подвижности ионов в решетке твердого тела в настоящее время еще недостаточно развиты и дифференцированы. Кроме того, при изучении подвижности до сих пор мало учитывали степень отклонения от стехиометрии в твердом теле. [1]
Подвижность кислорода и каталитическая активность окислов в отношении реакций окисления. [2]
Подвижность кислорода на поверхности серебра тесно связана с подвижностью поверхностных слоев самого металла. [3]
Подвижность кислорода и каталитическая активность окислов в отношении реакций окисления. [4]
Подвижность кислорода решетки легко обнаружить по изотопному кислородному обмену. Результаты работ Винтера [13], Т. В. Борескова и Л. А. Касаткиной [14], Камерона и других [15], а также наши экспериментальные данные показали, что при температурах каталитического процесса на Mn02, V05, Cu. Аналогичное комплексообразование наблюдается и на металлах серебре и платине, покрытых кислородом. Исследование изотопного обмена углекислого газа, содержащего О18 или смеси С02 016018, подтверждает предположение об образовании такого комплекса на поверхности. На рис. 4 показаны диаграмма скоростей кислородного обмена с С02 на различных катализаторах и для сравнения - скорости изотопного обмена С02 при реакции этилена с тяжелым кислородом. Из этих данных следует, что скорости изотопного обмена С02 без реакции в 2 - 3 раза выше, чем в условиях окислительного процесса. [5]
О подвижности кислорода окислов и кинетике кислородного обмена. [6]
Мерой подвижности кислорода, по их мнению, может служить способность ванада-тов самопроизвольно выделять кислород при кристаллизации с образованием ванадил-ванадатов. [7]
Обмен и подвижность кислорода, серы и азота. [8]
 |
Изотопный обмен кислорода на серебре и платине. [9] |
Какова же подвижность кислорода на поверхности серебра и платины. За 150 мин при 420 на платине обменивается до пяти монослоев кислорода. Вероятно, кислород, прочно связанный с поверхностью, не участвует в реакциях каталитического окисления. [10]
При повышении температуры подвижность кислорода решетки растет и, тем самым, возрастает активность катализатора, о чем свидетельствуют результаты опытов, проведенных при разных объемных скоростях потока газа-носителя. Параллельно с окислительным дегидрированием протекают также реакции миграции двойной связи и z / uc - ягранс-изомеризации. Особо следует отметить чрезвычайно низкие температуры ( около 100), при которых делается заметным образование дивинила. [12]
В табл. 25 дана характеристика подвижности кислорода на различных катализаторах; данные получены на основании изучения гетерообмена кислорода. [13]
Можно было предположить, лО чем больше подвижность кислорода окисла, тем - яри более низкой температуре реакция начинает осуществляться по окислительно-восстановительному механизму. [14]
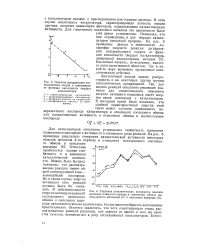 |
Скорость дегидратации изо.| Удельная каталитическая активность окислов., металлов четвертого периода в отношении обмена молекулярного кислорода ( / и окисления водорода ( / /. [15] |
Страницы: 1 2 3 4