Подвижность - водород
Cтраница 2
Это должно усиливать подвижность водорода оксимной группы и приводить к большей растворимости соединений металлов с бензоилметилдиодсимом по сравнению с их диметилдиоксиматами. [16]
В связи с малой подвижностью водорода в аустените граница сплавления оказывается как бы барьером, у которого накапливается большое количество водорода, поступающего в несплошности, где он ассоциирует в молекулы и перестает быть диффузионно-подвижным. Постепенно в таких несплошностях возрастает давление молекулярного водорода в связи с дальнейшим поступлением атомарного водорода и образованием новых молекул. Накопление диффузионно-подвижного, а также молекулярного водорода в несплошностях отрицательно сказывается на сопротивляемости стали разрушениям и способствует образованию трещин - отколов по зоне сплавления. [17]
Небольшая разница в подвижностях водорода сульфогидрильных групп исследованных ароматических и алифатических меркаптанов, по-видимому, достаточна для более интенсивного протекания реакций между гидроперекисями и ароматическими меркаптанами и соответственного увеличения их ингибирующего эффекта по сравнению с ингибирующим эффектом децил - и додецилмеркаптанов. Последнее также подтверждается небольшим различием в ингибирующих свойствах бензил - и фенилэтилмер-каптанов. [18]
Кислотность гумусовых веществ обусловлена подвижностью водорода, входящего в состав карбоксильных, фенольных и спиртовых гидро-ксильных групп. Эта подвижность проявляется в способности водорода замещаться металлами с образованием солеобразных соединений, а также в способности образовать эфиры со спиртами. Наиболее подвижен водород карбоксилов. Он количественно реагирует ( титруется) с карбонатами и ацетатами и наиболее легко вступает в реакции этерификации. Менее подвижен водород фенольных групп. Он титруется только едкой щелочью и трудно этерифицируется. Еще менее реакционно способен водород спиртового гидроксила. [19]
Химические свойства спиртов определяются подвижностью водорода гидроксогруппы. Водород гидроксила более подвижен, чем атомы водорода, непосредственно связанные с атомом углерода, например в метане. [20]
При смещении электронной плотности повышается подвижность водорода в р-положении, который благодаря отрицательному иону ( например, 1 -) легко отщепляется. Галогениды легко разлагаются в указанном выше порядке, потому что их способность отщеплять водород в р-положении велика и соответствует этому же порядку. [21]
При смещении электронной плотности повышается подвижность водорода в р-положении, и благодаря отрицательному иону ( например, 1 -) он легко отщепляется. Галогениды легко разлагаются в указанном выше порядке, потому что их способность отщеплять водород в Р - положении велика и соответствует этому же ряду. [22]
И в этой реакции сказывается подвижность водорода в группе - СН3 под влиянием соединенного с ней карбо-нила. [23]
Возможность металлирования углеводорода зависит от подвижности водорода в нем, от того, какой металл участвует в реакции и от условий ее проведения. Металлирование осуществляют действием расплавленного или измельченного металла. [24]
Электроноакцепторное влияние атома галогена увеличивает подвижность водорода в - положении и тем самым облегчает ено-лизацию. Не исключено, однако, что наряду с таким механизмом одновременно происходит частичное непосредственное замещение атомов водорода. [25]
И в этой реакции сказывается подвижность водорода в группе - СН3 под влиянием соединенного с ней карбо-нила. [26]
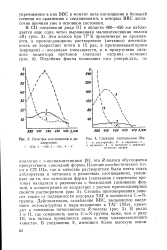 |
Спектры поглощения Ilia. [27] |
Степень протонирования зависит также от подвижности водорода ТАГ и основности C N-группы. [28]
Ацетон присоединяется ( за счет подвижности водорода метальных групп в щелочной среде) к этиленовой связи акрнло-нитрила. Происходит так называемое цианэтилирование. В зависимости от условий реакции ацетон может присоединить от одной до шести молекул акрилонитрила. [29]
Легкость протекания указанных реакций зависит от подвижности водорода в молекуле карбонильного соединения: чем более подвижен водород, тем с большей легкостью протекает реакция с бис ( тиофосфорил) дисульфидами. [30]
Страницы: 1 2 3