Автопротолиз
Cтраница 2
Константа автопротолиза муравьиной кислоты17 так велика ( pKs 6 2), что эта кислота оказывается непригодной в качестве среды для титрования. Однако это не исключает возмож - ности применения муравьиной кислоты в смесях с растворителями с низкой диэлектрической проницаемостью. Серная кислота, подобно муравьиной, имеет высокую константу автопротолиза ( pKs 3 85) и высокую диэлектрическую проницаемость. И хотя эта кислота почти не используется как среда для титрования, она может найти применение при спектрофотометриче-ских определениях. [16]
Константы автопротолиза многих неводных растворителей меньше ( табл. 3), чем у воды, поэтому в неводных растворах соли в значительно меньшей степени подвергаются сольволизу по сравнению с водными растворами. При титровании в неводных растворах это проявляется в увеличении скачков титрования, так как шкала рН неводных растворителей больше, чем у воды. [17]
Константа автопротолиза трибутилфосфата и константы диссоциации изучаемых нитросоединений в среде трибутилфосфата неизвестны. Мы определили потенциалы буферных ( полунейтрализованных) растворов нитрометана, 1 1-динитробутана и тринитрометана в трибутилфосфате по методике работы [10] и получили соответственно значения: 790; 245; 275 мв. [18]
Скорость автопротолиза метансульфоновой кислоты достаточно высока, чтобы обходиться без вспомогательного электролита. Добавка хлористого аммония, который реагирует с растворителем с образованием хлористого водорода и метансульфоната аммония, уменьшает сопротивление раствора. [19]
Скорость автопротолиза метансуль-фоновой кислоты достаточно высока, чтобы обходиться без вспомогательного электролита. Добавка хлористого аммония, который реагирует с растворителем с образованием хлористого водорода и метансульфбната аммония, уменьшает сопротивление раствора. [20]
Величина константы автопротолиза ( ионного произведения) растворителя Ks, являющаяся важнейшей термодинамической константой растворителя. [21]
Поэтому равновесие автопротолиза обусловливает эффект нивелирования сольвосистемы. [22]
Приведенное выше уравнение автопротолиза схематично. На самом деле в реакции самодиссоциации принимают участие ассо-циаты молекул уксусной кислоты. При этом образуются более сложные сольватированные ионы лиония [ Н п СНзСОО) ] и ионы лиата [ Н п - 1 ( СНзСОО) п - ] -, что указывает на способность уксусной кислоты выступать в роли донора протона и акцептора собственного аниона. [23]
Поскольку при реакции автопротолиза образуются как катионы, так и анионы растворителя, константа автопротолиза может служить мерой дифференцирующей способности растворителя. Если KSH растворителя сравнительно велика, то это означает, что нивелирующий эффект препятствует существованию в этом растворителе кислот и оснований, значительно различающихся по силе. И, наоборот, если константа автопротолиза невелика, то можно говорить о наличии кислот и оснований различной силы, что подтверждают четко различающиеся кривые титрования. [24]
Различие в константах автопротолиза и некоторых других свойств растворителей приводит к тому, что растворенные в них вещества проявляют свойства, отличающиеся от свойств, проявляемых в водных растворах. Особенно заметно изменяются свойства слабых кислот и слабых оснований. [25]
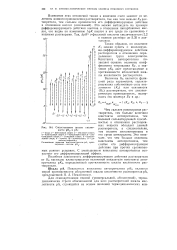 |
Сопоставление шкалы кислот - растворитель, а следовательно. [26] |
С уменьшением константы автопротолиза возрастает его дифференцирующий эффект. [27]
При протекании реакции автопротолиза (4.7) одновременно с образованием одного иона лиония образуется один ион лиата. [28]
При протекании реакции автопротолиза (4.3) одновременно с образованием одного иона лиония образуется один ион лиата. [29]
Страницы: 1 2 3 4