Закон - аррениус
Cтраница 1
Закон Аррениуса был открыт эмпирическим путем, так что, не вдаваясь пока в смысл величины Е, можно сказать, что она определяет степень зависимости константы скорости реакции ( а следовательно, и самой реакции) от температуры. Чем больше величина Е, тем больше возрастает скорость реакции при повышении температуры на одинаковое AT. [1]
Закон Аррениуса был открыт эмпирическим путем, так что, не вдаваясь пока в смысл величины Е, можно сказать, что она определяет степень зависимости константы скорости реакции ( а следовательно, и самой скорости реакции) от температуры. Чем больше величина Е, тем больше возрастает скорость реакции при увеличении температуры. Легко также сделать вывод, что при Е 0 скорость реакции не зависит от температуры. [2]
Закон Аррениуса устанавливает связь скорости химической реакции и ее температуры. [3]
Закон Аррениуса имеет следующее физическое толкование. [4]
 |
Определение энергии активации. [5] |
Закон Аррениуса имеет теоретическое толкование, вытекающее из законов статистической физики. [6]
Закону Аррениуса, имеющему эмпирическое происхождение, был дано два объяснения: термодинамическое и статистическое. [7]
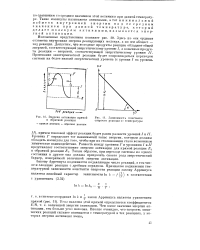 |
Энергия активации прямой.| Зависимость константы скорости реакции от температуры. [8] |
Закону Аррениуса подчиняется подавляющее число реакций, в том числе и сложные реакции с дробным порядком. [9]
Сравнивая закон Аррениуса и уравнение Больцмана, легко заметить, что обе зависимости выражаются экспоненциальными функциями. Заманчиво было предположить, что в химическую реакцию при столкновении вступают не все молекулы, а только те, которые обладают избыточной энергией. Тогда Е в уравнении (1.10) показывает значение избыточной энергии, которое обеспечивает протекание химической реакции при столкновении молекул. [10]
Сравнивая закон Аррениуса и уравнение Больцмана, легко заметить, что обе зависимости имеют одинаковый характер: обе выражаются экспоненциальной функцией. Заманчиво было сделать предположение ( и Аррениус сделал его) о том, что в реакцию при столкновении вступают не все молекулы, а только те, которые обладают энергией, превышающей среднее значение энергии молекул. Тогда Е в уравнении ( 1 - 21) - избыточная по сравнению со средней энергия, обладая которой, молекулы будут реагировать при столкновении. [11]
Применение закона Аррениуса к сложным химическим реакциям, строго говоря, неправомерно, однако опыт показывает, что происходит хорошее совпадение с экспериментом. [12]
Согласно закону Аррениуса, основания освобождают в воде гидроксильные ионы. [13]
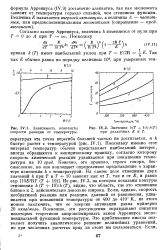 |
Зависимость константы скорости реакции от температуры.| Значения k ( T - f Ю при различных. и Г. [14] |
Согласно закону Аррениуса, величина k изменяется от нуля при Т 0 до А при Т - оо. [15]
Страницы: 1 2 3 4