Закон - аррениус
Cтраница 3
Это отклонение от закона Аррениуса связано с вкладом пограничной диффузии в общий диффузионный поток. Коэффициент пограничной диффузии на 3 - 5 порядков больше коэффициента объемной диффузии. Однако эта разница уменьшается с повышением температуры. [31]
Рассмотрим некоторые следствия закона Аррениуса. [32]
Формула (1.60) аналогична закону Аррениуса для скорости газовых реакций. Как известно, в случае газовых реакций активационный барьер преодолевается за счет избыточной кинетической энергии сталкивающихся частиц. [33]
Скорость превращения по закону Аррениуса в значительной степени зависит от температуры. Расстояние, на котором образуется первый локальный температурный максимум, является весьма важной мерой скорости преобразования профиля температуры к своей конечной форме для ламинарного пламени, в котором локальный максимум представляется почти внезапным скачком во фронте пламени. [34]
Соотношение (4.3) называется законом Аррениуса и является одним из важнейших в кинетике. [35]
Таким образом, уже закон Аррениуса в форме, принятой теорией переходного состояния, непосредственно указывал на существование двух факторов, от которых зависит скорость реакции - энергетического и энтропийного. [36]
В этих границах ни закон Аррениуса, ни формулы ( 25) и ( 27) неприменимы. При пропитке пентахлордифенилом они справедливы только при температурах выше 70 - 80 С. При более низких температурах заметно повышается вязкость хлордифенила, а в определенных границах с их повышением увеличивается срок службы конденсаторов. [37]
При всех конечных концентрациях закон Аррениуса для k не соблюдается, но наблюдающиеся во всех случаях температурные коэффициенты соответствуют величине видимой энергии активации, значительно превышающей 22 ккал / моль. [38]
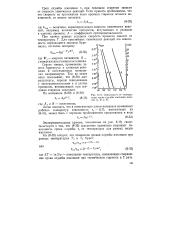 |
Зависимость от темпера. [39] |
Строго говоря, применение закона Аррениуса к сложным реакциям в изоляционных материалах неправомерно. Тем не менее опыт показывает, что ( 8 - 30) дает результаты, хорошо совпадающие с экспериментальными и в случае процессов, возникающих при тепловом старении изоляции. [40]
Эта эмпирическая формула соответствует закону Аррениуса. [41]
Цитируемое положение - это не закон Аррениуса, а правило - Вант-Гоффа, гораздо менее точное. Но и этим правилом принимается, что с увеличением температуры на 10 ускорение реакции может быть в 2 - 4 раза. Таким образом прогноз более чем неточен. [42]
К: к вычисляется из закона Аррениуса. [43]
Скорость реакции разложения СаСО3 подчиняется закону Аррениуса, она пропорциональна разности между равновесным давлением двуокиси углерода и давлением, поддерживаемым в шахте печи. Лимитирующей стадией процесса диссоциации является скорость образования кристаллических зародышей окиси кальция, которая, в свою очередь, зависит от скорости диффузии ионов металла. Более благоприятные условия для зарождения кристаллов СаО создаются при повышении температуры. [44]
А зависит от температуры по закону Аррениуса с энергией активации 75 ккал. [45]
Страницы: 1 2 3 4