Закон - электронейтральность
Cтраница 1
 |
Схема распределения зарядов в поле центрального иона. [1] |
Закон электронейтральности справедлив не только для раствора в целом, но и для любого заданного элемента его объема, достаточно большого по сравнению с размерами иона. [2]
Учтем закон электронейтральности раствора: нужно добавить к реагентам два иона ОН -, так как эта реакция протекает в щелочной среде. [3]
Далее необходимо выполнить закон электронейтральности - суммарное число зарядов продуктов реакции должно быть равно суммарному числу зарядов исходных веществ. [4]
При этом в силу закона электронейтральности возникает равное количество валентных катионных мест, чем объясняется увеличение электропроводности. [5]
Это равновесие вместе с законом электронейтральности сводит число компонентов до трех. [6]
В основе окислительно-восстановительных процессов лежит закон электронейтральности: если одно вещество окисляется, отдавая определенное количество электронов, то одновременно какое-либо другое вещество должно восстанавливаться, принимая все эти электроны. Этот закон всегда соблюдается при окислительно-восстановительных процессах. [7]
Для всей системы должен выполняться закон электронейтральности: общее число положительных зарядов в системе должно быть равно общему числу отрицательных зарядов. Поэтому справедливо следующее равенство: - число катионовХза - ряд катиона число анионовХзарОД аниона. [8]
Этот обмен происходит в стехиометрических соотношениях, так как при нем должен соблюдаться закон электронейтральности. [9]
Этот обмен происходит в стехио метрических соотношениях, так как при нем должен соблюдаться закон электронейтральности. [10]
Простейшим примером может служить обмен двух ионов на сильных ионитах, когда в силу закона электронейтральности их суммарная концентрация в грамм-эквивалентах ( но не в количестве частиц) остается постоянной. Не менее общим случаем является диффузия частиц в сорбентах, имеющих сложную микрострук - ТУРУ. [11]
Если два растворенных электролита не имеют общего иона, то система четырехкомпонентна, так как закон электронейтральности дает только одну взаимосвязь для любого числа видов ионов. В присутствии более чем двух видов ионов закон электронейтральности однозначно не определяет соотношение концентраций отдельных видов ионов, он только устанавливает для них определенные пределы. [12]
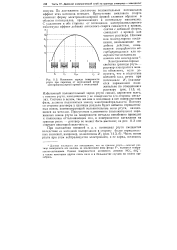 |
Изменение заряда поверхности. [13] |
Система в целом, так же как и входящая в нее поверхностная фаза, должны подчиняться закону электронейтральности. Поэтому со стороны раствора у границы раздела будет избыток отрицательных ионов, компенсирующий положительные ионы ртути, находящиеся на металле. [14]
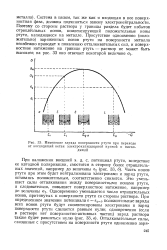 |
Изменение заряда поверхности ртути при переходе от восходящей ветви электрокапиллярной кривой к нисходящей. [15] |
Страницы: 1 2 3