Закон - электронейтральность
Cтраница 2
Система в целом, так же как и входящая в нее поверхностная фаза, должны подчиняться закону электронейтральности. Поэтому со стороны раствора у границы раздела будет избыток отрицательных ионов, компенсирующий положительные ионы ртути, находящиеся на металле. Присутствие одноименно ( положительно) заряженных ионов ртути на поверхности металла неизбежно приводит к появлению отталкивательных сил, и поверхностное натяжение на границе ртуть - раствор не может быть высоким; на рис. 33 оно отвечает некоторой величине аг. [16]
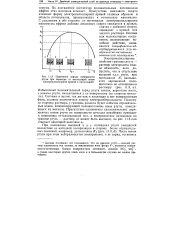 |
Изменение заряда поверхности. [17] |
Система в целом, так же как и входящая в нее поверхностная фаза, должны подчиняться закону электронейтральности. Поэтому со стороны раствора у границы раздела будет избыток отрицательных ионов, компенсирующий положительные ионы ртути, находящиеся на металле. [18]
Эти три вида частиц, однако, не независимы между собой, так как существуют определенные соответствующие закону электронейтральности связи между концентрациями положительных и отрицательных ионов. [19]
Можно было бы попытаться оправдать предположение о растворах замещения ( или внедрения) указанием на то обстоятельство, что появление одного избыточного ( сверх 50 %) иона кислорода в решетке требует по законам электронейтральности перехода двух ионов железа в трехвалентное состояние. Но и в этом случае, как легко показать, произойдет не уменьшение, а увеличение параметра решетки. [20]
Отправными моментами теории диффузии двух или более электролитов в общих растворах являются принципы, изложенные в разд. Однако из закона электронейтральности даже для ионов одинаковой зарядности не следует, что они благодаря взаимодействию диффундируют с одинаковой скоростью, так как, если в растворе присутствует более двух видов ионов с разными под-вижностями, электронейтральность реализуется не обязательно при одинаковых скоростях пар ионов. Каждому виду ионов может соответствовать своя, отличная от других скорость переноса. Однако преобладающее взаимодействие между диффундирующими ионами с различной подвижностью и в этих условиях должно обеспечить перенос со скоростями, соответствующими соблюдению электронейтральности. Другое, термодинамическое, взаимодействие имеет меньшее значение. [21]
Из приведенных выше уравнений мы можем заметить, что как и при всех других реакциях, точно так же и при реакциях окисления и восстановления арифметическая сумма электрических зарядов в одной части химического уравнения всегда равна арифметической сумме электрических зарядов в другой. Этот закон называется законом электронейтральности. [22]
Концентрации отдельных ионов в воде, мг / кг ( или мг-экв / кг), определяют методами химического анализа. Правильность проведения анализа должна подтверждаться выполнением закона электронейтральности XX 1 - Х мг-экв / кг. [23]
Если два растворенных электролита не имеют общего иона, то система четырехкомпонентна, так как закон электронейтральности дает только одну взаимосвязь для любого числа видов ионов. В присутствии более чем двух видов ионов закон электронейтральности однозначно не определяет соотношение концентраций отдельных видов ионов, он только устанавливает для них определенные пределы. [24]
Если вещество в одном из обоих растворителей диссоциировано, то ионы и недиссоциированная часть распределяются между обоими слоями, но уже не независимо друг от друга. Действительно, добавочным условием здесь служит требование закона электронейтральности о равенстве ( - -) и ( -) зарядов в каждом слое. [25]
Электролитами называют вещества, которые в растворе или расплаве распадаются на ионы - электрически заряженные частицы, способные к самостоятельному существованию в этих средах. Количество ионов каждого знака определяется стехиометрическими коэффициентами в формуле электролита при соблюдении закона электронейтральности, в соответствии с которым сумма положительных зарядов должна быть равна сумме отрицательных. Таким образом, несмотря на наличие ионов раствор остается электронейтральным. [26]
Система, состоящая из q компонентов, имеет q2 коэффициентов диффузии. В случае диффузии электролита q есть число независимых компонентов, полученное после учета закона электронейтральности. [27]
Важным отличием аэрозолей от жидких дисперсных систем является отсутствие электронейтральности системы в целом. Суспензии, эмульсии, лиозоли в макроколичествах не имеют заряда, в них соблюдается закон электронейтральности. Аэрозоль даже в больших количествах может обладать значительным статическим зарядом, а седиментация приводит к его неравномерному распределению в системе, что создает серьезные трудности при рассмотрении закономерностей изменения свойств аэрозолей. [28]
Важным отличием аэрозолей от жидких дисперсных систем является отсутствие электронейтральности в системе в целом. Суспензии, эмульсии, лиозоли в макроколичествах не имеют заряда, в них соблюдается закон электронейтральности. Аэрозоль даже в больших количествах может обладать значительным статическим зарядом, а седиментация приводит к его неравномерному распределению в системе, что создает серьезные трудности при рассмотрений закономерностей изменения свойств аэрозолей. [29]
 |
Остов из анионных комплексов. [30] |
Страницы: 1 2 3