Закон - идеальный газ
Cтраница 2
Поскольку иллюстрация законов идеальных газов относится к физическому практикуму, то в данном руководстве они не описываются. [16]
Отступление от законов идеальных газов становится тем более значительным, чем ниже температура и выше давление. [17]
Отклонения от двухмерного закона идеального газа вызваны тем, что молекулы имеют определенный размер. [19]
К подчиняется законам идеальных газов. [20]
При высоких давлениях закон идеального газа не выполняется. Здесь необходимо пользоваться уравнениями Ван-дер - Ваальса, Битти - Бриджмена или же вириальными коэффициентами. В условиях высокого и сверхвысокого вакуума закон идеального газа справедлив. [21]
В пределах применимости законов идеальных газов общее давление газовой смеси подчиняется закону Дальтона: обшре давление смеси газов равно сумме тех индивидуальных давлений, которыми обладал бы каждый ее компонент, если бы он один и при той же температуре занимал такой же объем, какой занимает вся смесь. [22]
В пределах соблюдения законов идеальных газов скорость звука не зависит от давления. При больших давлениях наступают отклонения. [23]
Если газ подчиняется законам идеальных газов, растворимость подчиняется закону Генри в нетермодинамической формулировке ( см. гл. VI) и сжимаемостью жидкости и изменением ее объема за счет растворенного газа можно пренебречь, то при постоянной температуре коэффициент Оствальда не зависит от давления. [24]
Если пар следует законам идеального газа, то внешняя работа испарения равна ЯГюш. [25]
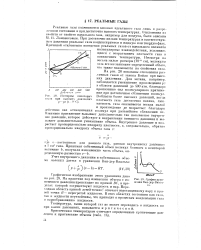 |
График уравнения Ван-дер - Ваал ь. [26] |
Реальные газы подчиняются законам идеального газа лишь в разреженном состоянии и при достаточно высоких температурах. При достаточно низких температурах и соответствующем давлении реальные газы конденсируются в жидкую или твердую фазу. [27]
Когда пар подчиняется закону идеальных газов, то следует применять уравнение ( 58) гл. Здесь же уравнение Клапейрона-Клаузиуса применяется к давлению пара жидкостей без каких-либо ограничении. В целях вычисления теплосодержания удобно представить уравнение ( 54) гл. [28]
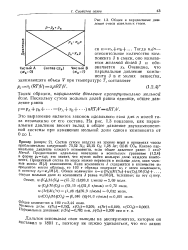 |
Общее и парциальные давления смеси идеальных газов. [29] |
Это выражение является законом идеального газа для п молей газа независимо от его состава. [30]
Страницы: 1 2 3 4
