Поле - лиганд
Cтраница 3
Сила поля лигандов ( А 10 /) в) мостиковых цианогрупп М - - CN - М со стороны атомов азота значительно меньше, чем со стороны атомов углерода. Так, для тетраэдрического окружения атомов никеля атомами азота в K2Ni [ Fe ( CN) 6 ] найдено [1556] Dq т 950 см 1; у ферро -, кобальти - и хромицианидов с мостиковы-ми цианогруппами сила поля лигандов со стороны атомов азота составляет всего Dg - 950 - 1010 см-1 [1556], тогда как со стороны атомов углерода величина Dq в несколько раз больше. [31]
 |
Состояния, возникающие из d2. [32] |
Теория поля лигандов, будучи эмпирической теорией, содержит параметры, представляющие собой разности энергий термов свободного атома. В случае - конфигурации наиболее важны термы 3Р и 3jF; разность их энергий будем обозначать символом В. [33]
 |
Характеристики ионов в октаэдрическом поле. [34] |
Действие поля лигандов оказывает влияние на самые различ ные свойства соединений rf - элементов. Следует учитывать, что ионы в водных растворах, как мы увидим ниже, образуют гид-ратные комплексы. [35]
Теория поля лигандов, предложенная первоначально для объяснения некоторых аномалий магнитных свойств ионов переходных металлов, нашла в дальнейшем и другие приложения. [36]
Теорию поля лигандов применяют к соединениям переходных металлов, где существенную роль играют cf - электроны. [37]
 |
Состояния, возникающие из d. [38] |
Теория поля лигандов, будучи эмпирической теорией, содержит параметры, представляющие собой разности энергий термов свободного атома. В случае - конфигурации наиболее важны термы 3Р и & Р разность их энергий будем обозначать сим-воло м В. [39]
Теория поля лигандов применима к тем металлам четвертого периода, которые обладают частично заполненными 3d - op - биталями. Одним из них является железо, которое мы уже рассматривали в свете теории валентных связей. [40]
Теория поля лигандов объединяет в той или иной мере идеи теории электростатического взаимодействия, метода валентных связей, теории кристаллического поля и метода молекулярных орбиталей. Теории поля лигандов и молекулярных орбиталей способны объяснить строение комплексов, энергию связи, магнитные свойства комплексных ионов, их окраску ( спектральные свойства), а также иногда объяснить реакционную способность комплексных соединений. [41]
 |
Изменение радиусов ионов в ряду Ca2t - Zn2. [42] |
Действие поля лигандов оказывает влияние на различные свойства соединений J-элементов. Следует иметь в виду, что ионы в водных растворах образуют гидратные комплексы. Ниже в качестве примера рассмотрена закономернсхггь изменения радиусов ионов в рядах ( / - элементов. [43]
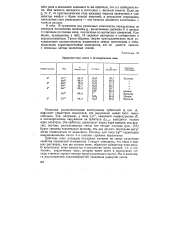 |
Характеристика ионов в октаэдрическом поле. [44] |
Действие поля лигандов оказывает влияние на самые различные свойства соединений d - элементов. Следует учитывать, что ионы в водных растворах, как мы увидим ниже, образуют гидратные комплексы. [45]
Страницы: 1 2 3 4 5