Электростатическое поле - катион
Cтраница 1
Электростатическое поле катионов воздействует не на молекулу субстрата, а на молекулу остаточной воды, подвергая ее гидролитической диссоциации, имеющей своим результатом возникновение кислотных ОН-групп. [1]
Рассмотрим влияние электростатического поля катиона. Величина - ( - Нк) ЕКн выражает напряженность поля катиона в направлении ОН-связи в точке расположения ядра атома водорода молекулы воды. Коэффициент Нк введен для учета экранирования ядра атома водорода электронами молекулы воды. Величина Екн вычисляется по закону Кулона на основе простых геометрических соображений и может служить относительной мерой электростатического воздействия на молекулу воды. [2]
Величина напряженности электростатического поля катиона Екн в направлении соответствующей связи в месте, где находится протон, для Mg2 больше, чем для любого двухвалентного иона переходного металла. [3]
Так как напряженность электростатического поля катионов щелочных металлов уменьшается с увеличением радиуса катиона, то в гидрате большого катиона Cs наличествует относительно слабое ион-дипольное взаимодействие, которое не приводит к полному разрушению структуры воды. Мало экранированное поле катиона действует на молекулы воды во второй гидратной сфере. Сильное взаимодействие катионов Li или Na с диполями воды приводит к обратному эффекту - созданию структуры гидрата и экранизации поля катиона. Поэтому действие этих катионов ограничено локальным разрушением структуры воды вблизи иона и образованием структуры гидратов. [4]
Был сделан вывод, что электростатическое поле катиона бария недостаточно сильное для того, чтобы вызвать диссоциацию. [6]
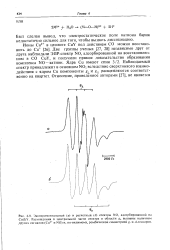
Зависимость положения высокочастотной полосы хемосорбированного СО2 от напряженности электростатического поля катиона и ее линейный характер, а также зависимость интенсивности полосы поглощения от количества двухвалентных катионов в адсорбционных полостях указывают на взаимодействие молекул СО2 с катионами. Компенсирующие катионы являются электроноак-цепторными центрами цеолита. [7]
 |
Возможные варианты расположения катиона относительно атомов кислорода иона - SO. [8] |
Это объясняет зависимость величины расщепления полосы от напряженности электростатического поля катиона, поскольку, чем сильнее поле, тем более поляризованным оказывается анион. Однако если имеет место такой механизм взаимодействия про-тивоионов, то величина расщепления должна быть тем больше, чем больше поляризуемость аниона. [9]
В водных растворах солей кобальта полярные молекулы воды под влиянием электростатического поля катиона ориентируются вокруг него, образуя гидратную оболочку из шести молекул и создают вокруг него электрическое поле определенной симметрии. Симметрия поля зависит от расположения молекул воды относительно центрального иона. [10]
В водных растворах солей кобальта полярные молекулы воды под влиянием электростатического поля катиона ориентируются вокруг него, образуя гндратную оболочку из шести молекул и создают вокруг него электрическое поле определенной симметрии. Симметрия поля зависит от расположения молекул воды относительно центрального иона. [11]
Процесс образования гидроксильных групп на поверхности катионных форм цеолитов количественно зависит от электростатического поля катионов. [12]
Наблюдаемые эффекты легко объяснить возрастанием числа протонов ( в результате диссоциации молекул воды под влиянием электростатического поля катионов) и увеличением общей кислотной силы. [13]
 |
Число и сила активных кислотных центров Н - формы цеолита Y. [14] |
Три главные реакции обусловливают бренстедовскую кислотность: разложение катионов NH4, диссоциация молекул гидратной воды под действием электростатического поля катионов, восстановление катионов под действием молекул реагентов. [15]
Страницы: 1 2 3