Полимеризация - этиленимин
Cтраница 2
Особым катализаторам полимеризации этиленимина является вода. Полимеризация в присутствии одной только воды [39, 40] протекает чрезвычайно медленно ( даже при повышенной температуре) и обычно прекращается на стадии тетрамера. Вода предложена [40] как специфический катализатор димеризации, тримеризации и тетрамеризации этиленимина. Добавление NaOH подавляет эту реакцию. [16]
Для предотвращения полимеризации исходного этиленимина образующейся НС1 реакцию проводят в присутствии щелочи. [17]
Особое место занимает полимеризация этиленимина в присутствии НСЮ4, HBF4, пикриновой и других кислот с весьма слабо нуклеофильными анионами. В этом случае оказывается справедливым первоначально высказанное предположение ( ом. Единственным побочным направлением в этом случае может быть сольволити-чвское ( гидролиз, алкоголиз) раскрытие этилениминных циклов, которое, однако, не вносит существенных изменений в кинетические закономерности. [18]
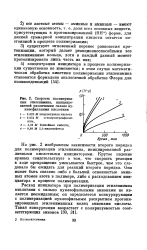 |
Скорость полимеризации этиленимина, инициированной различными сильно ну-клеофильными кислотами. [19] |
Расход инициатора при полимеризации этиленимина кислотами с сильно нуклеофильными анионами не является неожиданным; он определяется конкурирующим с полимеризацией нуклеофильным раскрытием протони-зированных этилениминных колец анионами кислоты. [20]
Разветвление цепей при полимеризации N-замещенных этилениминов, приводящее к образованию четвертичной аммониевой структуры ( блокирующей инициатор), может рассматриваться как кинетический обрыв этой полимеризации. Невысокий молекулярный вес поли - алкил-этилениминов, однако, наводит на мысль и об истинном обрыве полимерных цепей. [21]
Подтверждение инверсионного механизма полимеризации этиленимина было получено Миноура и др. [20], а также Цубояма [45] при исследовании полимеризации оптических изомеров пропиленимина и гексенимина. [22]
Различия в скоростях полимеризации этиленимина, инициированной различными сильно нуклеофильными кислотами ( рис. 2), могут быть связаны с различиями в скоростях побочных реакций анионов этих кислот с эти-ленимином. Наиболее определенную форму эти различия приобретают для сильных кислот ( серной, ге-толуолсульфо-кислоты, монохлоруксусной), с одной стороны, и слабых ( уксусной, бензойной, 2 4-дихлорфенола) - с другой. Тщательное исследование этих реакций Барбом [22] показало, что если в случае сильных кислот кинетическое течение деструкции инициатора согласуется с их полной ионизацией в растворе этиленимина, то кинетическим закономерностям полимеризации в присутствии слабых кислот удовлетворяет предположение об образовании ионных пар. [23]
В отношении механизма полимеризации этиленимина не существует единства мнений. Немецкие авторы [7, 16, 43] отстаивают механизм конденсационной полимеризации, который предполагает промежуточное образование продукта присоединения катализатора с раскрытием цикла этиленимина ( например, в случае НС1 - гидрохлорида р-хлорэтиламина) и включает две стадии: внутримолекулярную инверсию ( стадия, определяющая скорость) и анионоид-ное расщепление. [24]
Таким образом, хотя полимеризация этиленимина является присоединительной полимеризацией и в каждый данный момент присутствует лишь небольшое число реакционноспособных ими-ниевых ионов, общий характер ее аналогичен процессу ступенчатой поликонденсации, в которой все молекулы имеют реак-ционноспособные группы в результате очень быстрого смещения равновесия водородных ионов между различными присутствующими основаниями. [25]
Природа реакции обрыва при полимеризации этиленимина окончательно не решена, хотя на первый взгляд представляется достаточно очевидной. Прогрессивное снижение скорости в ходе превращения, как уже отмечалось, может быть связано с прогрессивным снижением концентрации реакционноспособных этиленими-ниевых катионов в результате конкуренции с ациклическими аминогруппами за кислотный инициатор. [26]
Было показано, что полимеризация этиленимина на Мо03 протекает со значительным периодом индукции ( от 40 до 80 мин в зависимости от температуры тренировки катализатора) и автокаталитическим ускорением. Изучение кинетики полимеризации этиленимина ( и окиси этилена для сравнения) на окиси алюминия и алюмосиликате весовым методом [40] показало, что после быстрой начальной адсорбции ( теплота адсорбции8 2 ккоиДиоль) мономера в количестве приблизительно монослоя ( - 10 - Б молъ / м при 25 С) начинается его полимеризация ( энергия активации 25 ккал / молъ) с постоянной скоростью. Полимер образует жидкую пленку на поверхности катализатора. [27]
Снижение скорости в ходе полимеризации этиленимина слабо нуклеофильными кислотами может быть связано с возрастающей в ходе превращения конкуренцией за обладание протонами между иминными циклами и аминными группировками полимера. Действительно, как видно из приводимого ниже сравнения, при низких степенях нейтрализации основность полимера приблизительно в 100 раз выше основности мономера. [28]
Матида [172, 173], исследовавший полимеризацию этиленимина, показал, что вода является инициатором реакции полимеризация, так же как двуокись углерода и различные кислоты. Полнэтиленлмин можно получить также из окиси этилена и мочевины при нагревании. Растворы полимера в воде обладают основными свойствами; при взаимодействии с формальдегидом образуется сшитый полимер. [29]
Матида [172, 173], исследовавший полимеризацию этиленимина, показал, что вода является инициатором реакции полимеризации, так же как двуокись углерода и различные кислоты. Полиэтиленимин можно получить также из окиаи этилена и мочевины при нагревании. Растворы полимера в воде обладают основными свойствами; при взаимодействии с формальдегидом образуется сшитый полимер. [30]
Страницы: 1 2 3 4