Полисиликат
Cтраница 2
Эти полисиликаты, очевидно, отличались от ранее упоминавшихся кристаллических полисиликатов натрия, однако имели сходные ионообменные свойства. Были также изучены системы, содержавшие ионы Li и К при различных соотношениях кремнезем-щелочь. Можно было ожидать образования кристаллических силикатов для литиевой системы, но результаты опытов автора настоящей монографии, выполненных с калиевой системой, свидетельствуют о том, что нерастворимые полисиликаты лития и калия нельзя получить при тех же условиях, при которых формируются полисиликаты натрия. [16]
Характерно, что при медленном естественном высушивании растворов полисиликатов ТБА в пленке кристаллы с этим же показателем преломления ( 1 475 - 1 480) обнаруживаются в большем или меньшем количестве среди аморфной фазы. ТБА на органическом стекле в пленке дает гигроскопичные невысыхающие мокрокристаллические пленки. Возможно, это и есть полученные Хоббелем высоководные клатратные структуры из несостарившихся растворов силикатов ТБА. Только ли старение растворов определяет выпадение высокомодульных маловодных кристаллов или какие-либо другие условия способствуют выпадению той или иной фазы - этот вопрос нуждается в уточнении. [17]
Следует также упомянуть большую группу неорганических полимеров - стеклообразных полисиликатов. Стеклоэмалевые материалы наносятся на защищаемые поверхности из расплава или оплавлением. Для закрепления они требуют температур, превышающих на 150 - 300 С рабочие температуры изделий. Присутствие в составе стекол щелочных добавок резко снижает изоляционные характеристики, особенно при повышенных температурах. [18]
Устойчивость этих мицелл ( которые могут быть названы коллоидными полисиликатами натрия) зависит от их ионного заряда. Заряд сильно понижается и кремнезем желатинизируется или осаждается, если присутствует растворимая соль. В основном заряд понижается из-за катиона. Как было показано Бакстером и Брайантом [44], в щелочных золях появляется коагуляция, особенно когда концентрация иона натрия доходит до 0 2 нормальной. [19]
В Технологическом институте были синтезированы и иссле дованы растворы полисиликатов ТЭА и ТБА силикатных модулей от 2 до 7, полученные растворением аэросила в концентрированных ( 30 - 35 %) растворах соответствующих гидроокисей. В табл. 18 представлены составы и физико-химические характеристики полученных растворов при 20 С. [20]
 |
Потери массы силиката ЧА ( SiO2 / NR412 5 в зависимости от температуры и времени сушки Числа у кривых - время сушки в минутах.| Время гелеобразования раствора силиката ЧА ( SiO2 / NR4 12 5 при. [21] |
Различные виды гидратации положительных и отрицательных частиц в растворах полисиликатов ЧА резко изменяют поляризационные свойства дисперсной фазы и обусловливают ее высокую УСТОЙЧИВОСТЬ к ассоциативным процессам. Известно [22], что для ионов четвертичного аммония характерна сильная гидрофобная гидратация, приводящая уже у ТБА к образованию клатратных структур и частиц, в противоположность положительной гидрата - Чии кремнезема. В целом это сочетание обусловливает низкую поляризуемость дисперсных частиц и тем самым высокую стабильность системы. [22]
Испарение воды из жидкого стекла также может вызвать разложение сложных полисиликатов натрия на более простые, сопровождающееся выпадением осадка. В обоих случаях модуль жидкого стекла изменяется. Использование жидкого стекла с изменяющимся модулем в производстве катализатора не рекомендуется, так как это приводит к повышенному растрсскивапию катализатора при сушке. [23]
Тило и Водтке664 установили, что разбавленный раствор HNOs разлагает полисиликат серебра ( Ag2SiO3) n с выделением кремневой кислоты. Жидкий NH3 на ( Ag2SiO3) n яе действует, однако раствор NH3 разлагает полисиликат на кремневую кислоту. Методом потенциометрического титрования исследованы равновесия в растворах силикатов с участием полисиликатных. [24]
Силикатными материалами называются материалы из смесей или сплавов силикатов, полисиликатов и алюмосиликатов. Так как главным в этом определении материала является признак его применимости, то к группе силикатных материалов относят и некоторые бессиликатные системы, применяемые для тех же целей, что и собственно силикаты. [25]
Так как силикат натрия в буровом растворе гидролизуется с образованием полисиликатов, а в результате взаимодействия с солями кальция выделяется химически активный гидрогель кремниевой кислоты, который при фильтрации остается в твердой фазе, то контролировать содержание силикатов в растворе невозможно. [26]
Теперь уже вполне очевидно, что может существовать целый ряд подобных полисиликатов, структура которых зависит от условий их образования и от присутствующих ионов. [27]
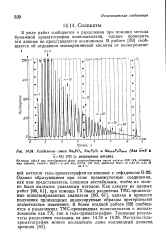 |
Разделение смеси Nu POt, NatPtOi и Naa zPnOsa i ( для л5 и п10 ( с разрешения автора. [28] |
В ряде работ сообщается о разделении при помощи метода бумажной хроматографии полисиликатов, однако проверить эти данные не представляется возможным. [29]
Когда, чтобы получить гидратированный гель, смешивают растворы алюмината и полисиликата, эти анионы, несомненно, вступают в реакцию полимеризации. Полученный в результате гель является аморфным и находится в предельно простом состоянии. Состав и структура такого геля определяются размером и структурой полимеризующихся частиц. Поскольку силикаты могут отличаться и по химическому составу и молекулярно-весовому распределению, структура гелей также может быть различной. Следовательно, процесс гелеобразования регулирует процесс образования ядер кристаллизации цеолитов. Это положение в общем подтверждается данными о размерах и морфологии кристаллов цеолитов, выращенных из гелей. Полученные кристаллы очень малы ( несколько микрон), однородны и часто имеют совершенную форму. Большая степень пересыщения ионами, содержащимися в геле, должна привести к быстрому гетерогенному ядрообразованию и возникновению большого числа центров кристаллизации. [30]
Страницы: 1 2 3 4