Положение - равновесие
Cтраница 2
 |
Фазовые траектории динамической системы второго порядка в окрестности узла.| Фазовые траектории динамической системы второго порядка в окрестности фокуса. [16] |
Положение равновесия называется фокусом. [17]
Положение равновесия называется седлом. Существуют четыре особые фазовые траектории, называемые сепаратрисами седла, по двум из которых изображающая точка приближается к положению равновесия, по двум другим - удаляется от него. На рис. 1 - 3 сепаратрисы проведены жирными линиями. [18]
Положения равновесия, находящиеся под этой кривой, являются седлами, и вопрос об их устойчивости отпадает. [19]
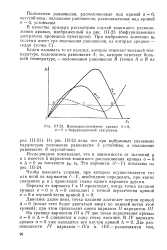 |
Взаиморасположение кривых А О, а 0 и бифуркационной диаграммы. [20] |
Положения равновесия, расположенные под кривой о О, неустойчивы; положения равновесия, расположенные над кривой а - 0, устойчивы. [21]
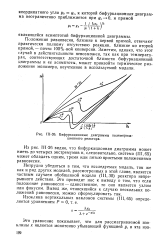 |
Бифуркационные диаграммы полимериза-ционного реактора. [22] |
Положения равновесия, близкие к первой прямой, отвечают практически полному отсутствию реакции, близкие ко второй прямой, - почти 100 % - ной конверсии. Заметим, однако, что этот случай в действительности невозможен, так как при температурах, соответствующих достаточной близости бифуркационной диаграммы и ее асимптоты, может произойти термическое разложение мономера, неучтенное в используемой модели. [23]
Положение равновесия не зависит от того, с какой стороны начинает протекать процесс. [24]
Положение равновесия в процессах термической диссоциации описанного вида ( когда диссоциация приводит к увеличению числа частиц) зависит от давления. Повышение давления всегда уменьшает степень диссоциации в таких процессах и, например, при атмосферном давлении все кривые рис. 33 6 будут смещены в сторону более высоких температур. [25]
Положение равновесия всегда зависит от внешних условий. Гак как внешние условия не могут сохраняться постоянно неизменными, следовательно, равновесие рано или поздно смещается или нарушается. [26]
Положение равновесия зависит от температуры. [27]
Положение равновесия сильно зависит от природы радикала R. Отметим, что константы равновесия относятся друг к другу как константы образования диодов. [28]
 |
Цис-транс-изомеры 1, 2-дихлорэтана ( ц - ди-польный момент в дебаях.| Син-анти-изомеры азобензола. [29] |
Положение равновесия определяется концентрацией ионов в растворе и в стекле. В кислых и слабо щелочных растворах это равновесие сдвинуто в сторону почти полного вытеснения ионов металла в стекле ионами Н, поэтому С. В сильно щелочных растворах равновесие сдвинуто в сторону почти полного замещения ионов 11 в стекле ионами металла. [30]
Страницы: 1 2 3 4