Положение - алкильная группа
Cтраница 1
Положение алкильной группы заметно влияет на устойчивость алкилзаме-щенных изомеров ряда адамантана. Однако общие закономерности, связывающие строение а л кил замещенных адамантанов ( как, впрочем, и других трициклических углеводородов) и их устойчивость в основном близки к закономерностям, отмеченным Для моноциклических и бициклических углеводородов. [1]
 |
Названия и сокращенные структурные формулы некоторых алкильных групп. [2] |
Положение алкильной группы вдоль углеродной цепочки указывают путем нумерации атомов углерода в цепочке. Так, название 2-метилпропан указывает на наличие в этом соединении метальной группы ( СН3), присоединенной ко второму атому углерода в пропановой ( трехуглеродной) цепочке. В общем случае нумерация атомов углерода в цепочке начинается с того ее конца, для которого положения алкильных групп указываются меньшими цифрами. [3]
Каково конформационное положение алкильных групп в цис-изомере продукта полного гидрирования ot - терпинена. [4]
 |
Данные масс-спектров ( 70 эВ некоторых инданов. [5] |
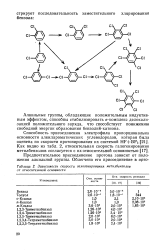
Изомеры по положению алкильной группы в гидрированном кольце тетралина масс-спектрометрически различаются легко. Для спектров 1-замещенных характерен максимальный пик иона [ М - алкил ], соответствующий выбросу заместителя в виде радикала, тогда как для многих 2-монозамещенных тетралинов основным в спектре является пик иона с tn / z 104, а пик иона [ М - алкил ] 4 имеет незначительную интенсивность. [6]
 |
Зависимость скорости галогенирования метилбензолов от относительной основности. [7] |
Предпочтительное присоединение протона зависит от положения алкильной группы. [8]
Легкость такой деформации существенно зависит от природы и положения алкильной группы в цикле. [9]
Температуры кипения фенолов находятся в прямой зависимости от положения алкильной группы по отношению к группе - ОН и определяются прежде всего положением водородного мостика. [10]
Точка помутнения у оксиэтилированных алкилфенолов зависит также от положения алкильной группы. [11]
Но в отличие от последних здесь гораздо большую роль играет положение алкильной группы относительно атома азота ядра пиридина. Это связано с тем, что благодаря неравномерности электронной плотности в кольце бензильный распад связи С-С в заместителе приводит к образованию в различной степени стабилизированных катионов. В 2-алкилпиридинах более выгодно расщепление в радикале 3-у - или у-б - С-С - связи ( или С - Н) с замыканием карбкатионного центра на нукле-офильный атом азота. [12]
Алкилхинолины ведут себя сходным образом, поэтому иногда трудно определить положение алкильной группы в пиридиновом или бензольном ядре. [13]
В продолжение предыдущих исследований, а также для выяснения влияния положения алкильной группы на процесс алкенилиронания нами предфинято исследование по алкенилированию i - и fi - метилнафталина бутадиеном в присутствии серной кислоты. [14]
При нагревании алкилбораны изомеризуются таким образом, что бор мигрирует к наименее замещенному положению алкильной группы. [15]
Страницы: 1 2 3 4